Autorisation de mise sur le marché des médicaments à usage ...
Autorisation de mise sur le marché des médicaments à usage ...
Autorisation de mise sur le marché des médicaments à usage ...
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
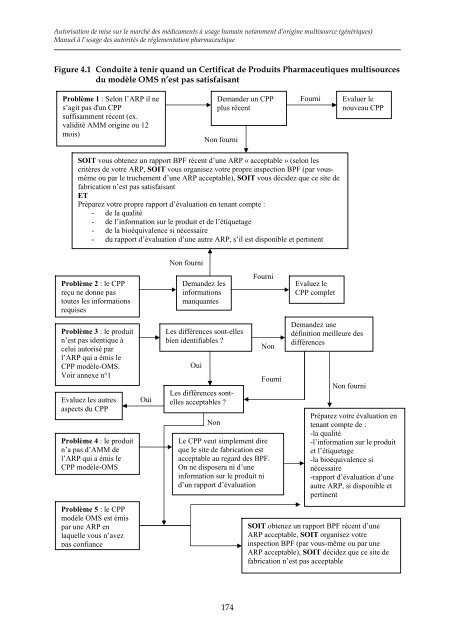
<strong>Autorisation</strong> <strong>de</strong> <strong>mise</strong> <strong>sur</strong> <strong>le</strong> <strong>marché</strong> <strong>de</strong>s <strong>médicaments</strong> <strong>à</strong> <strong>usage</strong> humain notamment d’origine multisource (génériques)Manuel <strong>à</strong> l'<strong>usage</strong> <strong>de</strong>s autorités <strong>de</strong> rég<strong>le</strong>mentation pharmaceutiqueFigure 4.1 Conduite <strong>à</strong> tenir quand un Certificat <strong>de</strong> Produits Pharmaceutiques multisourcesdu modè<strong>le</strong> OMS n’est pas satisfaisantProblème 1 : Selon l’ARP il nes’agit pas d'un CPPsuffisamment récent (ex.validité AMM origine ou 12mois)Deman<strong>de</strong>r un CPPplus récentNon fourniFourniEvaluer <strong>le</strong>nouveau CPPSOIT vous obtenez un rapport BPF récent d’une ARP « acceptab<strong>le</strong> » (selon <strong>le</strong>scritères <strong>de</strong> votre ARP, SOIT vous organisez votre propre inspection BPF (par vousmêmeou par <strong>le</strong> truchement d’une ARP acceptab<strong>le</strong>), SOIT vous déci<strong>de</strong>z que ce site <strong>de</strong>fabrication n’est pas satisfaisantETPréparez votre propre rapport d’évaluation en tenant compte :- <strong>de</strong> la qualité- <strong>de</strong> l’information <strong>sur</strong> <strong>le</strong> produit et <strong>de</strong> l’étiquetage- <strong>de</strong> la bioéquiva<strong>le</strong>nce si nécessaire- du rapport d’évaluation d’une autre ARP, s’il est disponib<strong>le</strong> et pertinentNon fourniProblème 2 : <strong>le</strong> CPPreçu ne donne pastoutes <strong>le</strong>s informationsrequisesDeman<strong>de</strong>z <strong>le</strong>sinformationsmanquantesFourniEvaluez <strong>le</strong>CPP comp<strong>le</strong>tProblème 3 : <strong>le</strong> produitn’est pas i<strong>de</strong>ntique <strong>à</strong>celui autorisé parl’ARP qui a émis <strong>le</strong>CPP modè<strong>le</strong>-OMS.Voir annexe n°1Evaluez <strong>le</strong>s autresaspects du CPPProblème 4 : <strong>le</strong> produitn’a pas d’AMM <strong>de</strong>l’ARP qui a émis <strong>le</strong>CPP modè<strong>le</strong>-OMSProblème 5 : <strong>le</strong> CPPmodè<strong>le</strong> OMS est émispar une ARP enlaquel<strong>le</strong> vous n’avezpas confianceOuiLes différences sont-el<strong>le</strong>sbien i<strong>de</strong>ntifiab<strong>le</strong>s ?OuiLes différences sontel<strong>le</strong>sacceptab<strong>le</strong>s ?NonNonLe CPP veut simp<strong>le</strong>ment direque <strong>le</strong> site <strong>de</strong> fabrication estacceptab<strong>le</strong> au regard <strong>de</strong>s BPF.On ne disposera ni d’uneinformation <strong>sur</strong> <strong>le</strong> produit nid’un rapport d’évaluationFourniDeman<strong>de</strong>z unedéfinition meil<strong>le</strong>ure <strong>de</strong>sdifférencesNon fourniPréparez votre évaluation entenant compte <strong>de</strong> :-la qualité-l’information <strong>sur</strong> <strong>le</strong> produitet l’étiquetage-la bioéquiva<strong>le</strong>nce sinécessaire-rapport d’évaluation d’uneautre ARP, si disponib<strong>le</strong> etpertinentSOIT obtenez un rapport BPF récent d’uneARP acceptab<strong>le</strong>, SOIT organisez votreinspection BPF (par vous-même ou par uneARP acceptab<strong>le</strong>), SOIT déci<strong>de</strong>z que ce site <strong>de</strong>fabrication n’est pas acceptab<strong>le</strong>174