Chemická termodynamika II
Chemická termodynamika II
Chemická termodynamika II
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
7.1.1 Základní typy s -f. diagramů u binárních systémů<br />
Na tomto místě si pro upřesnění důležitých termínů provedeme rekapitulaci základních<br />
s-i diagramůu binárních systémů. Systém s eutektickým bodemje nejčastěji<br />
se vyskytujícím základním typem. Vyskytuje se všude tam, kde látky v tuhém stavu<br />
jsou nemísite1né, což jest velnů častý případ zvláště u systémů, které jsou tvořeny<br />
organickými látkami. Opačný případ, tj. existence tuhého roztoku, kdy se molekuly<br />
obou složek mohou vzájemně zastupovat v krystalové mřížce, vyžaduje nejen velmi<br />
podobnou strukturu molekul (pokud se týče elektronové hustoty), ale i velrrů podobnou<br />
velikost molekuly. Tak např. K+Rb jsou mísitelné v tuhé fázi, ale Na+Rb už<br />
ne.<br />
350<br />
T<br />
300<br />
a<br />
b<br />
E<br />
, "<br />
270 , ~<br />
D<br />
X A<br />
A<br />
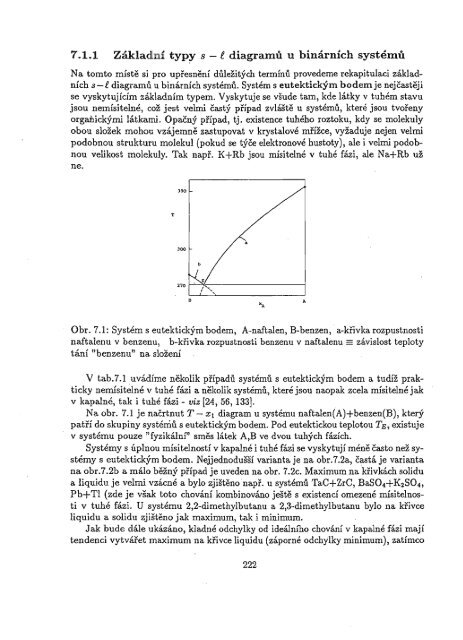
Obr. 7.1: Systém s eutektickým bodem, A-naftalen, B-benzen, . a-křivka rozpustnosti<br />
naftalenu v benzenu, b-křivka rozpustnosti benzenu v naftalenu == závislost teploty<br />
tání "benzenu" na složení<br />
.1<br />
,. I<br />
V tab.7.1 uvádíme několik případů systémů s eutektickým bodem a tudíž prakticky<br />
nemísitelné v tuhé fázi a několik systémů, které jsou naopa.k zcela mísitelné jak<br />
v kapalné, tak i tuhé fázi - viz [24, 56, 133J.<br />
Na. obr. 7.1 je načrtnut T - Xl diagram u systému naftalen(A)+benzen(B), který<br />
patří do skupiny systémů s eutektickým bodem. Pod eutektickou teplotou TE, existuje<br />
v systému pouze "fyzikálnÍ" směs látek A,B ve dvou tuhých fázích.<br />
Systémy s úplnou mísitelností v kapalné i tuhé fázi se vyskytují méně často než systémy<br />
s eutektickým bodem. Nejjednodušší varianta je na obr.7.2a, častá-je varianta<br />
na obr.7.2b a málo běžný případ je uveden na obr. 7.2c. Maximum na křivkáchsolidu<br />
a liquidu je velmi vzá.cné a bylo zjištěno např. u systémů TaC+ZrC, BaS04+K 2 S04,<br />
Pb+TI (zde je však toto chování kombinováno ještě s existencí omezené mísitelnosti<br />
v tuhé fázi. U systému 2,2-dimethylbutanu a 2,3-dimethylbutanu bylo na křivce<br />
liquidu a solidu zjištěno jak maximum, tak i minimum.<br />
Jak bude dále ukázáno, kladné odchylky od ideálního chování v kapalné fázi mají<br />
tendenci vytvářet maximum na křivce liquidu (zá.porné odchylky minimum), zatímco<br />
222