Chemická termodynamika II
Chemická termodynamika II
Chemická termodynamika II
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
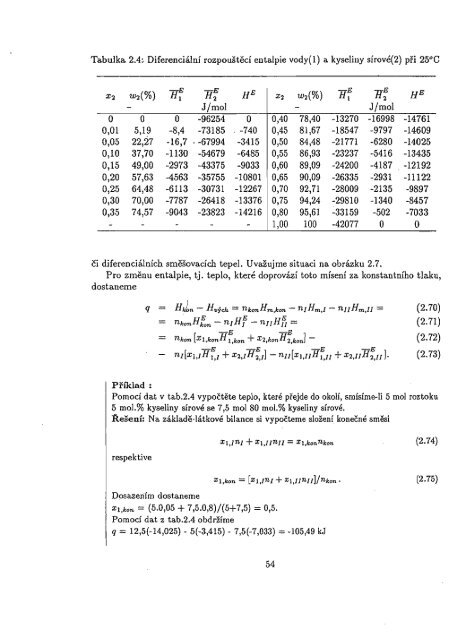
Tabulka 2.4:. Diferenciální rozpouštěcí entalpie vody( 1) a kyseliny sírové(2) při 25°C<br />
Xz wz(%)<br />
-E<br />
Hl<br />
-E<br />
Hz HE Xz wz(%)<br />
-E<br />
Hl<br />
-E<br />
Hz H E<br />
Jfmol<br />
Jfmol<br />
O O -96254 0,40 78,40 -13270 -16998 -14761<br />
0,01 5,1~ -8,4 -73185 . -740 0,45 81,67 -18547 -9797 -14609<br />
°<br />
°<br />
0,05 22,27 -16,7 . -67994 -3415 0,50 84,48 -21771 -6280 -14025<br />
0,10 37,70 -1130 -54679 -6485 0,55 86,93 -23237 -5416 -13435<br />
0,15 49,00 -2973 -43375 -9033 0,60 89,09 -24200 -4187 -12192<br />
0,20 57,63 -4563 -35755 -10801 0,65 90,09 -26335 -2931 -11122<br />
0,25 64,48 -6113 -30731 -12267 0,70 92,71 -28009 -2135 -9897<br />
0,30 70,00 -7787 -26418 -13376 0,75 94,24 -29810 -1340 -8457<br />
0,35 74,57 -9043 -23823 -14216 0,80 95,61 -33159 -502 -7033<br />
1,00 100 -42077<br />
° °<br />
či diferenciálních směšovacích tepel. Uvažujme situaci na obrázku 2.7.<br />
Pro změnu entalpie, tj. teplo, které doprovází toto mísení za konstantního tlaku,<br />
dostaneme<br />
q =<br />
)<br />
H~n - Hvých = nkonHm,kon - nlHm,I - nl1Hm,Il =<br />
= n~onHfon - nlHf - nlIHfI =<br />
-E -E<br />
= nkon [Xl,konH l,kon + XZ,kon H z,konJ -<br />
-E -E -E -E<br />
nl[Xl,/H1,/ + Xz,t H 2,1] - nJI[XI,l1 H I,JI + X2,IJH2,Il J.<br />
(2.70)<br />
(2.71)<br />
(2.72)<br />
(2.73)<br />
Příklad:<br />
Pomocí dat v tab.2.4 vypočtěte teplo, které přejde do okolí, smísíme-li 5 mol roztoku<br />
5 mol.% kyseliny sírové se 7,5 mol 80 mol.% kyseliny sírové.<br />
ftešení: Na zá.kladě·lá.tkové bilance si vypočteme složení konečné směsi<br />
respektive<br />
(2.74)<br />
(2.75)<br />
Dosazením dost.aneme<br />
XI,kon = (5.0,05 + 7,5.0,8)/(5+7,5) = 0,5.<br />
Pomocí dat z tab.2,4 obdržíme<br />
Iq = 12,5(-14,025) - 5(-3,415) - 7,5(-7,033) = -105,49 kJ<br />
54