Biochemische Charakterisierung der siRNA-vermittelten Erkennung ...
Biochemische Charakterisierung der siRNA-vermittelten Erkennung ...
Biochemische Charakterisierung der siRNA-vermittelten Erkennung ...
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
elative Fluoreszenz<br />
relative Fluoreszenz<br />
5 Ergebnisse<br />
keine Auswirkung auf die Anzahl und die Geschwindigkeit <strong>der</strong> Phasen <strong>der</strong> Assoziation besitzt.<br />
Dieses Ergebnis konnte mit den Substraten 19mer-FAM und sLam-Alexa488 bestätigt werden.<br />
Im nächsten Schritt wurde die Dissoziation des binären Komplexes aus NHA-hAgo2 und P-<br />
as2B-FAM bzw. OH-as2B-FAM unter pre-steady state Bedingungen untersucht. Zwar konnte<br />
für die erste Phase bereits k -1 indirekt ermittelt werden, jedoch wurden die Daten durch ein<br />
Experiment bestätigt, bei dem zeitaufgelöst die Verdrängung von as2B-FAM aus dem binären<br />
Komplex durch einen 100-fachen Überschuss nicht-markierter asLam beobachtet wurde (siehe<br />
Abbildung 5.28).<br />
Zunächst fällt auf, dass die durch Verdrängung hervorgerufene Signalzunahme in beiden<br />
Fällen deutlich geringer ist als die Abnahme während <strong>der</strong> Bildung des binären Komplexes.<br />
Dies spricht dafür, dass nur etwa 20 % von P-as2B-FAM bzw. OH-as2B-FAM verdrängt werden<br />
können. Durch die geringere Amplitude ist das Signal-zu-Rausch-Verhältnis kleiner als bei <strong>der</strong><br />
Beobachtung <strong>der</strong> Assoziation und die ermittelten Werte weisen einen gröÿeren Fehler auf.<br />
Allerdings war die Güte <strong>der</strong> Daten ausreichend für eine mathematische Auswertung.<br />
Es zeigte sich, dass auch die Dissoziation mindestens ein dreiphasiger Prozess ist. Durch Auswertung<br />
<strong>der</strong> experimentellen Daten mit einer dreifach exponentiellen Gleichung ergaben sich<br />
k -1 = 14,7 (± 2,5) s -1 , k -2 = 0,17 (± 0,02) s -1 und k -3 = 0,0066 (± 0,0001) s -1 für den Zerfall eines<br />
NHA-hAgo2/P-as2B-FAM-Komplexes. Für die Dissoziation von NHA-hAgo2 und OH-as2B-<br />
FAM wurden als Ratenkonstanten k -1 = 10,9 (± 15,9) s -1 , k -2 = 1,7 (± 0,3) s -1 und k -3 = 0,0094<br />
NHA<br />
hAgo2<br />
A<br />
1,02<br />
B<br />
1,06<br />
1,04<br />
1,01<br />
1,04<br />
1,02<br />
1,02<br />
1,08<br />
1,04<br />
1<br />
1<br />
1<br />
0,98<br />
1<br />
0,96<br />
0,96<br />
0 0,2 0,4 0,6 0,8 1<br />
0,92<br />
0 0,2 0,4 0,6 0,8 1<br />
0,99<br />
0 200 400 600 800 1000<br />
Zeit (s)<br />
0,98<br />
0 200 400 600 800 1000<br />
Zeit (s)<br />
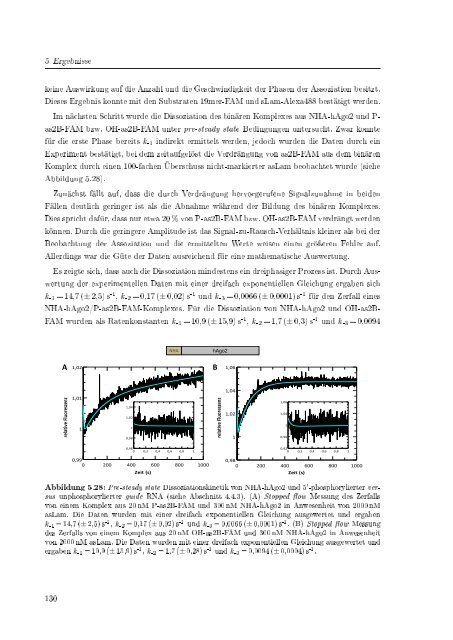
Abbildung 5.28: Pre-steady state Dissoziationskinetik von NHA-hAgo2 und 5'-phosphorylierter versus<br />
unphosphorylierter guide RNA (siehe Abschnitt 4.4.3). (A) Stopped ow Messung des Zerfalls<br />
von einem Komplex aus 20 nM P-as2B-FAM und 300 nM NHA-hAgo2 in Anwesenheit von 2000 nM<br />
asLam. Die Daten wurden mit einer dreifach exponentiellen Gleichung ausgewertet und ergaben<br />
k -1 = 14,7 (± 2,5) s -1 , k -2 = 0,17 (± 0,02) s -1 und k -3 = 0,0066 (± 0,0001) s -1 . (B) Stopped ow Messung<br />
des Zerfalls von einem Komplex aus 20 nM OH-as2B-FAM und 300 nM NHA-hAgo2 in Anwesenheit<br />
von 2000 nM asLam. Die Daten wurden mit einer dreifach exponentiellen Gleichung ausgewertet und<br />
ergaben k -1 = 10,9 (± 15,9) s -1 , k -2 = 1,7 (± 0,28) s -1 und k -3 = 0,0094 (± 0,0004) s -1 .<br />
130