Biochemische Charakterisierung der siRNA-vermittelten Erkennung ...
Biochemische Charakterisierung der siRNA-vermittelten Erkennung ...
Biochemische Charakterisierung der siRNA-vermittelten Erkennung ...
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
elative Fluoreszenz<br />
relative Fluoreszenz<br />
relative Fluoreszenz<br />
relative Fluoreszenz<br />
5.8 <strong>Charakterisierung</strong> <strong>der</strong> target RNA-Bindung durch den binären hAgo2/guide RNA-Komplex<br />
3,6<br />
GST<br />
hAgo2<br />
3,6<br />
3,4<br />
3,2<br />
3<br />
2,8<br />
A<br />
1,8<br />
1,6<br />
1,4<br />
1,2<br />
1<br />
2,6<br />
0 200 400 600 0,8<br />
800 1000<br />
Zeit (s) 0 200 400 600 800 1000<br />
Zeit (s)<br />
3,4<br />
3,2<br />
B<br />
1,02<br />
3<br />
guide und target RNA<br />
0,98<br />
komplementär<br />
2,8<br />
guide und target RNA<br />
nicht komplementär<br />
0,96<br />
2,6<br />
0 200 400 600 800 1000<br />
Zeit (s) 0,94<br />
1<br />
guide und target RNA<br />
komplementär<br />
guide und target RNA<br />
nicht komplementär<br />
0,92<br />
0 0,1 0,2 0,3 0,4 0,5<br />
Zeit (s)<br />
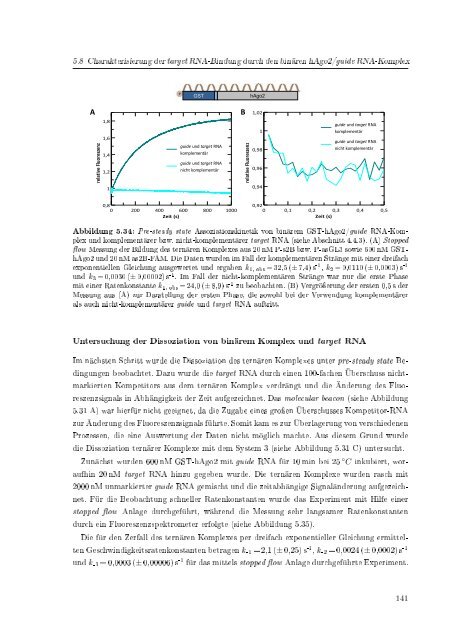
Abbildung 5.34: Pre-steady state Assoziationskinetik von binärem GST-hAgo2/guide RNA-Komplex<br />
und komplementärer bzw. nicht-komplementärer target RNA (siehe Abschnitt 4.4.3). (A) Stopped<br />
ow Messung <strong>der</strong> Bildung des ternären Komplexes aus 20 nM P-s2B bzw. P-asGL3 sowie 600 nM GSThAgo2<br />
und 20 nM as2B-FAM. Die Daten wurden im Fall <strong>der</strong> komplementären Stränge mit einer dreifach<br />
exponentiellen Gleichung ausgewertet und ergaben k 1, obs = 32,5 (± 7,4) s -1 , k 2 = 0,0110 (± 0,0003) s -1<br />
und k 3 = 0,0030 (± 0,00002) s -1 . Im Fall <strong>der</strong> nicht-komplementären Stränge war nur die erste Phase<br />
mit einer Ratenkonstante k 1, obs = 24,0 (± 8,9) s -1 zu beobachten. (B) Vergröÿerung <strong>der</strong> ersten 0,5 s <strong>der</strong><br />
Messung aus (A) zur Darstellung <strong>der</strong> ersten Phase, die sowohl bei <strong>der</strong> Verwendung komplementärer<br />
als auch nicht-komplementärer guide und target RNA auftritt.<br />
Untersuchung <strong>der</strong> Dissoziation von binärem Komplex und target RNA<br />
Im nächsten Schritt wurde die Dissoziation des ternären Komplexes unter pre-steady state Bedingungen<br />
beobachtet. Dazu wurde die target RNA durch einen 100-fachen Überschuss nichtmarkierten<br />
Kompetitors aus dem ternären Komplex verdrängt und die Än<strong>der</strong>ung des Fluoreszenzsignals<br />
in Abhängigkeit <strong>der</strong> Zeit aufgezeichnet. Das molecular beacon (siehe Abbildung<br />
5.31 A) war hierfür nicht geeignet, da die Zugabe eines groÿen Überschusses Kompetitor-RNA<br />
zur Än<strong>der</strong>ung des Fluoreszenzsignals führte. Somit kam es zur Überlagerung von verschiedenen<br />
Prozessen, die eine Auswertung <strong>der</strong> Daten nicht möglich machte. Aus diesem Grund wurde<br />
die Dissoziation ternärer Komplexe mit dem System 3 (siehe Abbildung 5.31 C) untersucht.<br />
Zunächst wurden 600 nM GST-hAgo2 mit guide RNA für 10 min bei 25 ◦ C inkubiert, woraufhin<br />
20 nM target RNA hinzu gegeben wurde. Die ternären Komplexe wurden rasch mit<br />
2000 nM unmarkierter guide RNA gemischt und die zeitabhängige Signalän<strong>der</strong>ung aufgezeichnet.<br />
Für die Beobachtung schneller Ratenkonstanten wurde das Experiment mit Hilfe einer<br />
stopped ow Anlage durchgeführt, während die Messung sehr langsamer Ratenkonstanten<br />
durch ein Fluoreszenzspektrometer erfolgte (siehe Abbildung 5.35).<br />
Die für den Zerfall des ternären Komplexes per dreifach exponentieller Gleichung ermittelten<br />
Geschwindigkeitsratenkonstanten betragen k -1 = 2,1 (± 0,25) s -1 , k -2 = 0,0024 (± 0,0002) s -1<br />
und k -3 = 0,0003 (± 0,00006) s -1 für das mittels stopped ow Anlage durchgeführte Experiment.<br />
141