- Seite 3 und 4:
3Einführung“Material, von spätl
- Seite 5 und 6:
Inhaltsverzeichnis1 Kristallstruktu
- Seite 7 und 8:
INHALTSVERZEICHNIS 74.3.1 Einleitun
- Seite 9 und 10:
Kapitel 1Kristallstrukturen1.1 Tran
- Seite 11 und 12:
1.1. TRANSLATIONSGITTER, SYMMETRIEN
- Seite 14 und 15:
14 KAPITEL 1. KRISTALLSTRUKTUREN1.2
- Seite 16 und 17:
16 KAPITEL 1. KRISTALLSTRUKTURENAbb
- Seite 18 und 19:
18 KAPITEL 1. KRISTALLSTRUKTURENAbb
- Seite 20 und 21:
20 KAPITEL 1. KRISTALLSTRUKTURENEs
- Seite 22 und 23:
22 KAPITEL 1. KRISTALLSTRUKTURENAbb
- Seite 24 und 25:
24 KAPITEL 1. KRISTALLSTRUKTURENAbb
- Seite 26 und 27:
26 KAPITEL 1. KRISTALLSTRUKTURENsei
- Seite 28 und 29:
28 KAPITEL 1. KRISTALLSTRUKTURENdie
- Seite 30 und 31:
30 KAPITEL 1. KRISTALLSTRUKTURENKri
- Seite 32 und 33:
32 KAPITEL 1. KRISTALLSTRUKTURENAbb
- Seite 34 und 35:
34 KAPITEL 1. KRISTALLSTRUKTURENAto
- Seite 36 und 37:
36 KAPITEL 1. KRISTALLSTRUKTURENAus
- Seite 38 und 39:
38 KAPITEL 1. KRISTALLSTRUKTURENAbb
- Seite 40 und 41:
40 KAPITEL 1. KRISTALLSTRUKTURENEnt
- Seite 42 und 43:
42 KAPITEL 1. KRISTALLSTRUKTURENfü
- Seite 44 und 45:
44 KAPITEL 1. KRISTALLSTRUKTURENPla
- Seite 46 und 47:
46 KAPITEL 1. KRISTALLSTRUKTURENEin
- Seite 48 und 49:
48 KAPITEL 1. KRISTALLSTRUKTURENden
- Seite 50 und 51: 50 KAPITEL 1. KRISTALLSTRUKTUREN
- Seite 52 und 53: 52 KAPITEL 2. STRUKTURBESTIMMUNGZwe
- Seite 54 und 55: 54 KAPITEL 2. STRUKTURBESTIMMUNGder
- Seite 56 und 57: 56 KAPITEL 2. STRUKTURBESTIMMUNGdie
- Seite 58 und 59: 58 KAPITEL 2. STRUKTURBESTIMMUNGV i
- Seite 60 und 61: 60 KAPITEL 2. STRUKTURBESTIMMUNGbei
- Seite 62 und 63: 62 KAPITEL 2. STRUKTURBESTIMMUNGnen
- Seite 64 und 65: 64 KAPITEL 2. STRUKTURBESTIMMUNGAbb
- Seite 66 und 67: 66 KAPITEL 2. STRUKTURBESTIMMUNG2.3
- Seite 68 und 69: 68 KAPITEL 2. STRUKTURBESTIMMUNGDie
- Seite 70 und 71: 70 KAPITEL 2. STRUKTURBESTIMMUNG•
- Seite 72 und 73: 72 KAPITEL 2. STRUKTURBESTIMMUNGAto
- Seite 74 und 75: 74 KAPITEL 2. STRUKTURBESTIMMUNGAbb
- Seite 76 und 77: 76 KAPITEL 2. STRUKTURBESTIMMUNGEne
- Seite 78 und 79: 78 KAPITEL 2. STRUKTURBESTIMMUNG3.
- Seite 80 und 81: 80 KAPITEL 2. STRUKTURBESTIMMUNGAus
- Seite 82 und 83: 82 KAPITEL 2. STRUKTURBESTIMMUNGAbb
- Seite 84 und 85: 84 KAPITEL 2. STRUKTURBESTIMMUNGAbb
- Seite 86 und 87: 86 KAPITEL 2. STRUKTURBESTIMMUNG
- Seite 88 und 89: 88 KAPITEL 3. MEHRSTOFFSYSTEMEAbbil
- Seite 91 und 92: 3.2. THERMODYNAMISCHE GRUNDLAGEN 91
- Seite 93 und 94: 3.2. THERMODYNAMISCHE GRUNDLAGEN 93
- Seite 95 und 96: 3.2. THERMODYNAMISCHE GRUNDLAGEN 95
- Seite 97 und 98: 3.2. THERMODYNAMISCHE GRUNDLAGEN 97
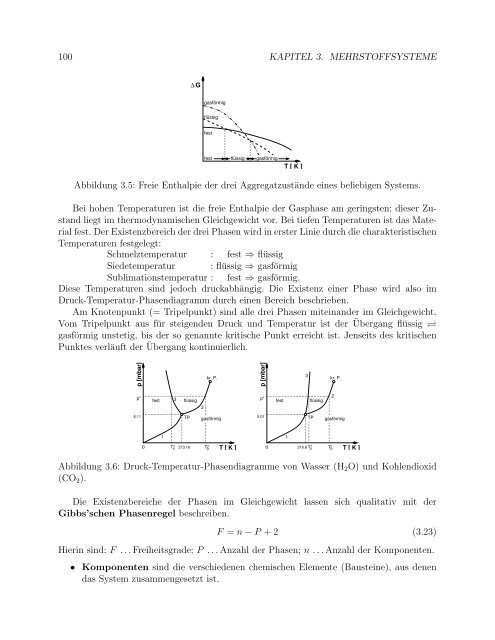
- Seite 99: 3.3. KONSTITUTIONSLEHRE 99Der Einfa
- Seite 103 und 104: 3.3. KONSTITUTIONSLEHRE 103tiefe T
- Seite 105 und 106: 3.3. KONSTITUTIONSLEHRE 105Analog s
- Seite 107 und 108: 3.3. KONSTITUTIONSLEHRE 107Das Hebe
- Seite 109 und 110: 3.3. KONSTITUTIONSLEHRE 109Allerdin
- Seite 111 und 112: 3.3. KONSTITUTIONSLEHRE 111und Liqu
- Seite 113 und 114: 3.3. KONSTITUTIONSLEHRE 113∆ GT 1
- Seite 115 und 116: 3.3. KONSTITUTIONSLEHRE 115Konzentr
- Seite 117 und 118: 3.3. KONSTITUTIONSLEHRE 117also die
- Seite 119 und 120: 3.4. REALE ZUSTANDSDIAGRAMME UND IH
- Seite 121 und 122: 3.4. REALE ZUSTANDSDIAGRAMME UND IH
- Seite 123 und 124: 3.4. REALE ZUSTANDSDIAGRAMME UND IH
- Seite 125 und 126: 3.4. REALE ZUSTANDSDIAGRAMME UND IH
- Seite 127 und 128: 3.4. REALE ZUSTANDSDIAGRAMME UND IH
- Seite 129 und 130: 3.4. REALE ZUSTANDSDIAGRAMME UND IH
- Seite 131 und 132: 3.4. REALE ZUSTANDSDIAGRAMME UND IH
- Seite 133 und 134: 3.4. REALE ZUSTANDSDIAGRAMME UND IH
- Seite 135 und 136: 3.5. DIFFUSION 13512 · 1.602 · 10
- Seite 137 und 138: 3.5. DIFFUSION 137Festkörper immer
- Seite 139 und 140: 3.5. DIFFUSION 139Wie erfolgt der M
- Seite 141 und 142: 3.5. DIFFUSION 141Austausch von Feh
- Seite 143 und 144: 3.5. DIFFUSION 143Abbildung 3.49: G
- Seite 145 und 146: 3.5. DIFFUSION 145Eine solche Anord
- Seite 147 und 148: 3.5. DIFFUSION 147Abbildung 3.52: P
- Seite 149 und 150: 3.6. ENTMISCHUNGSVORGÄNGE 149Abbil
- Seite 151 und 152:
3.6. ENTMISCHUNGSVORGÄNGE 151Abbil
- Seite 153 und 154:
3.6. ENTMISCHUNGSVORGÄNGE 153Abbil
- Seite 155 und 156:
3.6. ENTMISCHUNGSVORGÄNGE 155Abbil
- Seite 157 und 158:
3.6. ENTMISCHUNGSVORGÄNGE 157• B
- Seite 159 und 160:
3.7. OBERFLÄCHEN UND GRENZFLÄCHEN
- Seite 161 und 162:
3.7. OBERFLÄCHEN UND GRENZFLÄCHEN
- Seite 163 und 164:
3.7. OBERFLÄCHEN UND GRENZFLÄCHEN
- Seite 165 und 166:
3.8. PRÄPARATIONSMETHODEN 165• K
- Seite 167 und 168:
3.8. PRÄPARATIONSMETHODEN 1673.8.6
- Seite 169 und 170:
Kapitel 4Makroskopische Eigenschaft
- Seite 171 und 172:
4.1. METALLE, HALBLEITER UND ISOLAT
- Seite 173 und 174:
4.1. METALLE, HALBLEITER UND ISOLAT
- Seite 175 und 176:
4.1. METALLE, HALBLEITER UND ISOLAT
- Seite 177 und 178:
4.1. METALLE, HALBLEITER UND ISOLAT
- Seite 179 und 180:
4.1. METALLE, HALBLEITER UND ISOLAT
- Seite 181 und 182:
4.1. METALLE, HALBLEITER UND ISOLAT
- Seite 183 und 184:
4.2. HALBLEITER 183Am unteren Bandr
- Seite 185 und 186:
4.2. HALBLEITER 185mit( ) 3/2 mkB T
- Seite 187 und 188:
4.2. HALBLEITER 187Das P-Atom stell
- Seite 189 und 190:
4.2. HALBLEITER 189die Zustände un
- Seite 191 und 192:
4.2. HALBLEITER 191derstand ist seh
- Seite 193 und 194:
4.2. HALBLEITER 193Abbildung 4.16:
- Seite 195 und 196:
4.3. MECHANISCHE EIGENSCHAFTEN 195A
- Seite 197 und 198:
4.3. MECHANISCHE EIGENSCHAFTEN 197w
- Seite 199 und 200:
4.3. MECHANISCHE EIGENSCHAFTEN 199D
- Seite 201 und 202:
4.3. MECHANISCHE EIGENSCHAFTEN 2014
- Seite 203 und 204:
4.3. MECHANISCHE EIGENSCHAFTEN 203A
- Seite 205 und 206:
4.3. MECHANISCHE EIGENSCHAFTEN 205h
- Seite 207 und 208:
4.3. MECHANISCHE EIGENSCHAFTEN 207
- Seite 209 und 210:
4.4. THERMISCHE EIGENSCHAFTEN 209sc
- Seite 211 und 212:
4.4. THERMISCHE EIGENSCHAFTEN 211Um
- Seite 213 und 214:
4.4. THERMISCHE EIGENSCHAFTEN 213(a
- Seite 215 und 216:
4.4. THERMISCHE EIGENSCHAFTEN 215er
- Seite 217 und 218:
4.4. THERMISCHE EIGENSCHAFTEN 21712
- Seite 219 und 220:
4.4. THERMISCHE EIGENSCHAFTEN 219au
- Seite 221 und 222:
4.4. THERMISCHE EIGENSCHAFTEN 221W
- Seite 223 und 224:
4.4. THERMISCHE EIGENSCHAFTEN 223(a
- Seite 225 und 226:
4.4. THERMISCHE EIGENSCHAFTEN 225Re
- Seite 227 und 228:
4.4. THERMISCHE EIGENSCHAFTEN 227be
- Seite 229 und 230:
4.4. THERMISCHE EIGENSCHAFTEN 229ge
- Seite 231 und 232:
4.4. THERMISCHE EIGENSCHAFTEN 231Da
- Seite 233 und 234:
4.5. MAGNETISCHE EIGENSCHAFTEN 233D
- Seite 235 und 236:
4.5. MAGNETISCHE EIGENSCHAFTEN 235A
- Seite 237 und 238:
4.5. MAGNETISCHE EIGENSCHAFTEN 237
- Seite 239 und 240:
4.5. MAGNETISCHE EIGENSCHAFTEN 239a
- Seite 241 und 242:
4.5. MAGNETISCHE EIGENSCHAFTEN 241M
- Seite 243 und 244:
4.5. MAGNETISCHE EIGENSCHAFTEN 243S
- Seite 245 und 246:
4.5. MAGNETISCHE EIGENSCHAFTEN 245m
- Seite 247 und 248:
4.5. MAGNETISCHE EIGENSCHAFTEN 247f
- Seite 249 und 250:
4.5. MAGNETISCHE EIGENSCHAFTEN 249D
- Seite 251 und 252:
4.5. MAGNETISCHE EIGENSCHAFTEN 251A
- Seite 253 und 254:
4.5. MAGNETISCHE EIGENSCHAFTEN 253R
- Seite 255 und 256:
4.5. MAGNETISCHE EIGENSCHAFTEN 255u
- Seite 257 und 258:
4.5. MAGNETISCHE EIGENSCHAFTEN 257V
- Seite 259 und 260:
4.5. MAGNETISCHE EIGENSCHAFTEN 259a
- Seite 261 und 262:
Anhang AModellbildung zur thermisch
- Seite 263 und 264:
∂S r∂VHier sind die 〈E r i
- Seite 265:
265D(E F ) bezeichnet die Zustandsd