PRINCÍPIOS SÍNTESE ORGÂNICA - CEFET-MG Campus Timóteo
PRINCÍPIOS SÍNTESE ORGÂNICA - CEFET-MG Campus Timóteo
PRINCÍPIOS SÍNTESE ORGÂNICA - CEFET-MG Campus Timóteo
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
A. Isenmann <strong>CEFET</strong>-<strong>MG</strong> <strong>Timóteo</strong> Princípios da Síntese Orgânica<br />
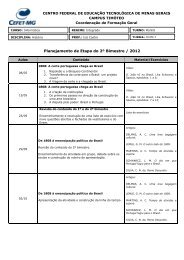
Figura 13. Os orbitais moleculares (MO) de 1,3,5-hexatrieno e sua ocupação por elétrons,<br />
no estado fundamental. Foi escolhida a conformação favorável à reação eletrocíclica. (Por<br />
fim de salvar espaço a gráfica não reproduz a certa posição relativa na escala energética.)<br />
Na figura acima estão representados todos os orbitais moleculares que se acharam por<br />
combinação linear para o 1,3,5-hexatrieno. Como cada carbono contribui com um elétron<br />
do tipo π, então temos em total 6 elétrons que podem ser distribuidos sobre esses MOs. A<br />
química da molécula depende basicamente destes elétrons π por serem mais energéticos<br />
que os elétrons σ, por sua vez responsáveis para as ligações C-H e C-C simples. Na<br />
situação mais favorável esses 6 elétrons ocupam os MOs de energia mais baixa, no caso Ψ1<br />
a Ψ3. Essa distribuição é chamada de estado fundamental. Mas sob incidência de energia,<br />
especialmente em forma de luz ultravioleta, um destes elétrons pode ser elevado a um MO<br />
mais alto. A probabilidade de elevar ao mesmo tempo dois elétrons a MOs mais altas,<br />
geralmente é muito pequena e portanto este caso não é discutido 121 . Note que no caso do<br />
1,3,5-hexatrieno todos os MOs têm energias diferentes, enquanto outras moléculas, por<br />
exemplo o benzeno, podem também dispor de MOs de energias idênticas, daí chamados de<br />
degenerados. Em caso de elétrons insuficientes esses MOs serão todos ocupados por<br />
somente um elétron, antes de colocar um par de elétrons em somente um MO (regra de<br />
Hund).<br />
O orbital do 1,3,5-hexatrieno de energia mais baixa é o Ψ1. Todos os lobos escuros<br />
mostram no mesmo sentido. Os elétrons que se encontram neste orbital têm muito espaço<br />
disponível (elétrons "moles"), na verdade são localizados entre todos os lobos da mesma<br />
cor. Note-se que o orbital Ψ1 tem um plano de nó (isto é, uma área onde a probabilidade de<br />
encontrar um elétron é zero) que coincide com o plano dos núcleos dos carbonos.<br />
Já o orbital Ψ2 tem uma série de lobos cuja parte escura mostra para cima e uma outra série<br />
cuja parte escura mostra para baixo. Aqui têm-se dois planos de nó: o plano dos núcleos<br />
mais um plano perpendicular a este, entre os átomos C3 e C4. O espaço disponível para os<br />
elétrons neste orbital é, portanto, menor do que no Ψ1. Em geral vale: prender elétrons num<br />
pequeno espaço é uma desvantagem energética (baixa polarizabilidade; elétrons "duros",<br />
compare p. 37). Então podemos afirmar que Ψ2 se encontra num nível energético mais alto<br />
do que o Ψ1. Assim para diante: o orbital molecular Ψ3 se caracteriza por ter três nós (no<br />
plano dos núcleos, entre C2 e C3 e entre C4 e C5), então fica num nível energético mais<br />
alto do que o Ψ2....<br />
Observação:<br />
No exemplo escolhido todos planos nodais se encontram entre os núcleos de carbono.<br />
Porém, existem também moléculas onde o plano de nó coincide com a posição de um<br />
núcleo. Essa situação podemos esperar em moléculas onde o número de átomos<br />
contribuintes ao sistema π é impar; em particular, isto são moléculas com heteroátomo cujo<br />
par de elétrons n (=não-ligante) participa no sistema π, ver p. 238 e questão 8 no anexo<br />
121 Note, porém, que na espectroscopia de UV-VIS este caso pode ser provocado, pela incidência de luz de<br />
altíssima intensidade, em forma de Laser. Daí falamos da espectroscopia eletrônica de dois fótons, para a qual<br />
valem outras regras de seleção do que se conhecem no método clássico de um só fóton.<br />
203