PRINCÍPIOS SÍNTESE ORGÂNICA - CEFET-MG Campus Timóteo
PRINCÍPIOS SÍNTESE ORGÂNICA - CEFET-MG Campus Timóteo
PRINCÍPIOS SÍNTESE ORGÂNICA - CEFET-MG Campus Timóteo
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
A. Isenmann <strong>CEFET</strong>-<strong>MG</strong> <strong>Timóteo</strong> Princípios da Síntese Orgânica<br />
H 3C<br />
O<br />
R<br />
H<br />
Nu -<br />
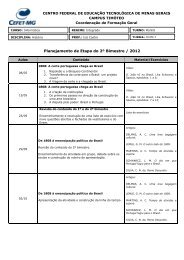
Conformação de Cram<br />
H3C O<br />
Nu -<br />
H<br />
R<br />
Conformação de Felkin<br />
Finalmente, o refinamento por Nguyen 145 incluiu a posição e os tamanhos dos lobos dos<br />
orbitais moleculares do agrupamento >C=O e levou em consideração o correto ângulo de<br />
ataque em compostos carbonilados (ver ângulo de Bürgi-Dunitz, p. 387).<br />
Embora da plausibilidade e da previsão correta de diastereoisômeros, esses modelos não<br />
são livres de exceções. Nestes todos exemplos foram considerados os efeitos estéricos,<br />
principalmente. Quando se sobrepõem efeitos eletrônicos, atuando entre o grupo em<br />
posição α, o nucleófilo atacante e o oxigênio do grupo carbonila, então podemos contar<br />
com desvios destes modelos. Também a presença de metais ácidos de Lewis, com poder de<br />
complexação, os produtos deviam das regras estabelecidas 146 . Existem também teorias e<br />
modelos sobre o efeito dos substituintes em posição β, em relação ao grupo carbonila 147 .<br />
3) Catálise assimétrica 148<br />
Síntese a partir de material pro-quiral, acelerando especificamente a formação de um dos<br />
possíveis enanciômeros. O centro pro-quiral geralmente é um carbono sp² (um grupo<br />
carbonila, como visto acima, ou um alqueno) no qual se adiciona um nucleófilo, tornando-o<br />
em um carbono sp³ sendo novo centro assimétrico. A estereosseletividade implica que o<br />
próprio catalisador tem que ser quiral e opticamente puro. A epoxidação de Sharpless<br />
apresentada a seguir é um exemplo desta estratégia; outros são:<br />
• Hidrogenação de epóxidos ou cetonas, com catalisadores de Ru ou Rh em forma de<br />
complexos com ligantes quirais (recorra p. 585 para a técnica, e p. 698, para os<br />
ligantes cabíveis do tipo fosfina). A hidrogenação assimétrica de uma olefina proquiral,<br />
usando um catalisador de Wilkinson com ligantes quirais do tipo fosfina, foi<br />
o trabalho pioneiro nesta área, para o qual W.S. Knowles (1968) ganhou o prêmio<br />
Nobel em 2001, junto a Sharpless.<br />
• No mesmo ano, Noyori conseguiu uma ciclopropanação em estireno 149 , ainda em<br />
baixo excesso enanciomêrico (somente 6%ee).<br />
145<br />
N.T. Anh, O. Eisenstein, J-M. Lefour, M.E. Dau, J.Am.Chem.Soc. 95 (1973) 6146.<br />
146<br />
Uma ótima abordagem sobre o desenvolvimento dos modelos de adições no grupo carbonila, encontra-se<br />
no site:<br />
http://evans.harvard.edu/pdf/smnr_2000-2001_Siska_Sarah.pdf (acesso em outubro de 2010)<br />
147<br />
D.A. Evans, M.J. Dart, J.L. Duffy, M.G. Yang, J.Am.Chem.Soc. 118 (1996) 4322.<br />
148<br />
As reações catalisadas por enzimas devem ser incluídas nesta categoria, também. Essa discussão, porém,<br />
fica fora do âmbito deste livro. Um exemplo é dado na p. Erro! Indicador não definido..<br />
149<br />
H. Nozaki, H. Takaya, S. Moriuti, R. Noyori, Homogeneous catalysis in the decomposition of diazo<br />
compounds by copper chelates: Asymmetric carbenoid reactions. Tetrahedron 24 (1968) 3655-3669.<br />
227