Principios de Neurociencia Haines 4a Ed_booksmedicos.org
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
256 Neurobiología <strong>de</strong> los sistemas<br />
Arteria<br />
vertebral<br />
PICA<br />
Eminencia<br />
<strong>de</strong><br />
Anterior<br />
Arteria vertebral<br />
Sistema anterolateral<br />
Espinal <strong>de</strong>l tngémino:<br />
Núcleo (porción interpolar)<br />
An le ñor<br />
Núcleo ambiguo<br />
Núcleo motor<br />
dorsal <strong>de</strong>l vago<br />
Plexo coroi<strong>de</strong>o<br />
Arteria cerebelosa<br />
posteroinferior (PICA)<br />
restiforme<br />
y tracto<br />
solitario<br />
Núcteos vestibulares:<br />
Infenor<br />
Vista RM/TC<br />
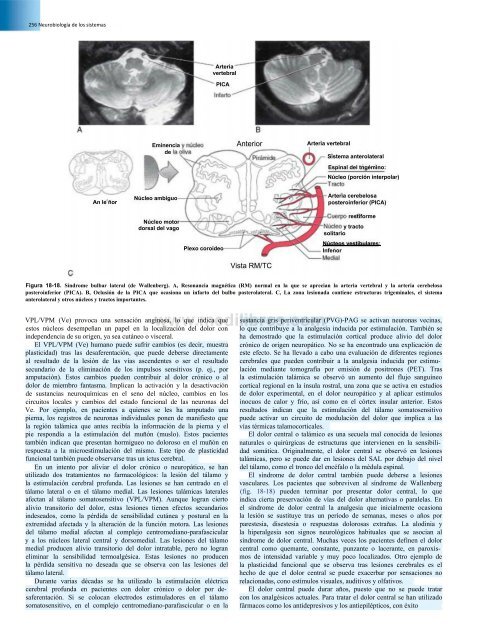
Figura 18-18. Síndrome bulbar lateral (<strong>de</strong> Wallenberg). A, Resonancia magnética (RM) normal en la que se aprecian la arteria vertebral y la arteria cerebelosa<br />
posteroinferior (PICA). B, Oclusión <strong>de</strong> la PICA que ocasiona un infarto <strong>de</strong>l bulbo posterolateral. C, La zona lesionada contiene estructuras trigeminales, el sistema<br />
anterolateral y otros núcleos y tractos importantes.<br />
VPL/VPM (Ve) provoca una sensación anginosa, lo que indica que<br />
estos núcleos <strong>de</strong>sempeñan un papel en la localización <strong>de</strong>l dolor con<br />
in<strong>de</strong>pen<strong>de</strong>ncia <strong>de</strong> su origen, ya sea cutáneo o visceral.<br />
El VPL/VPM (Ve) humano pue<strong>de</strong> sufrir cambios (es <strong>de</strong>cir, muestra<br />
plasticidad) tras las <strong>de</strong>saferentación, que pue<strong>de</strong> <strong>de</strong>berse directamente<br />
al resultado <strong>de</strong> la lesión <strong>de</strong> las vías ascen<strong>de</strong>ntes o ser el resultado<br />
secundario <strong>de</strong> la eliminación <strong>de</strong> los impulsos sensitivos (p. ej., por<br />
amputación). Estos cambios pue<strong>de</strong>n contribuir al dolor crónico o al<br />
dolor <strong>de</strong> miembro fantasma. Implican la activación y la <strong>de</strong>sactivación<br />
<strong>de</strong> sustancias neuroquímicas en el seno <strong>de</strong>l núcleo, cambios en los<br />
circuitos locales y cambios <strong>de</strong>l estado funcional <strong>de</strong> las neuronas <strong>de</strong>l<br />
Ve. Por ejemplo, en pacientes a quienes se les ha amputado una<br />
pierna, los registros <strong>de</strong> neuronas individuales ponen <strong>de</strong> manifiesto que<br />
la región talámica que antes recibía la información <strong>de</strong> la pierna y el<br />
pie respondía a la estimulación <strong>de</strong>l muñón (muslo). Estos pacientes<br />
también indican que presentan hormigueo no doloroso en el muñón en<br />
respuesta a la microestimulación <strong>de</strong>l mismo. Este tipo <strong>de</strong> plasticidad<br />
funcional también pue<strong>de</strong> observarse tras un ictus cerebral.<br />
En un intento por aliviar el dolor crónico o neuropático, se han<br />
utilizado dos tratamientos no farmacológicos: la lesión <strong>de</strong>l tálamo y<br />
la estimulación cerebral profunda. Las lesiones se han centrado en el<br />
tálamo lateral o en el tálamo medial. Las lesiones talámicas laterales<br />
afectan al tálamo somatosensitivo (VPL/VPM). Aunque logran cierto<br />
alivio transitorio <strong>de</strong>l dolor, estas lesiones tienen efectos secundarios<br />
in<strong>de</strong>seados, como la pérdida <strong>de</strong> sensibilidad cutánea y postural en la<br />
extremidad afectada y la alteración <strong>de</strong> la función motora. Las lesiones<br />
<strong>de</strong>l tálamo medial afectan al complejo centromediano-parafascicular<br />
y a los núcleos lateral central y dorsomedial. Las lesiones <strong>de</strong>l tálamo<br />
medial producen alivio transitorio <strong>de</strong>l dolor intratable, pero no logran<br />
eliminar la sensibilidad termoalgésica. Estas lesiones no producen<br />
la pérdida sensitiva no <strong>de</strong>seada que se observa con las lesiones <strong>de</strong>l<br />
tálamo lateral.<br />
Durante varias décadas se ha utilizado la estimulación eléctrica<br />
cerebral profunda en pacientes con dolor crónico o dolor por <strong>de</strong>saferentación.<br />
Si se colocan electrodos estimuladores en el tálamo<br />
somatosensitivo, en el complejo centromediano-parafascicular o en la<br />
sustancia gris periventricular (PVG)-PAG se activan neuronas vecinas,<br />
lo que contribuye a la analgesia inducida por estimulación. También se<br />
ha <strong>de</strong>mostrado que la estimulación cortical produce alivio <strong>de</strong>l dolor<br />
crónico <strong>de</strong> origen neuropático. No se ha encontrado una explicación <strong>de</strong><br />
este efecto. Se ha llevado a cabo una evaluación <strong>de</strong> diferentes regiones<br />
cerebrales que pue<strong>de</strong>n contribuir a la analgesia inducida por estimulación<br />
mediante tomografía por emisión <strong>de</strong> positrones (PET). Tras<br />
la estimulación talámica se observó un aumento <strong>de</strong>l flujo sanguíneo<br />
cortical regional en la ínsula rostral, una zona que se activa en estudios<br />
<strong>de</strong> dolor experimental, en el dolor neuropático y al aplicar estímulos<br />
inocuos <strong>de</strong> calor y frío, así como en el córtex insular anterior. Estos<br />
resultados indican que la estimulación <strong>de</strong>l tálamo somatosensitivo<br />
pue<strong>de</strong> activar un circuito <strong>de</strong> modulación <strong>de</strong>l dolor que implica a las<br />
vías térmicas talamocorticales.<br />
El dolor central o talámico es una secuela mal conocida <strong>de</strong> lesiones<br />
naturales o quirúrgicas <strong>de</strong> estructuras que intervienen en la sensibilidad<br />
somática. Originalmente, el dolor central se observó en lesiones<br />
talámicas, pero se pue<strong>de</strong> dar en lesiones <strong>de</strong>l SAL por <strong>de</strong>bajo <strong>de</strong>l nivel<br />
<strong>de</strong>l tálamo, como el tronco <strong>de</strong>l encéfalo o la médula espinal.<br />
El síndrome <strong>de</strong> dolor central también pue<strong>de</strong> <strong>de</strong>berse a lesiones<br />
vasculares. Los pacientes que sobreviven al síndrome <strong>de</strong> Wallenberg<br />
(fig. 18-18) pue<strong>de</strong>n terminar por presentar dolor central, lo que<br />
indica cierta preservación <strong>de</strong> vías <strong>de</strong>l dolor alternativas o paralelas. En<br />
el síndrome <strong>de</strong> dolor central la analgesia que inicialmente ocasiona<br />
la lesión se sustituye tras un período <strong>de</strong> semanas, meses o años por<br />
parestesia, disestesia o respuestas dolorosas extrañas. La alodinia y<br />
la hiperalgesia son signos neurológicos habituales que se asocian al<br />
síndrome <strong>de</strong> dolor central. Muchas veces los pacientes <strong>de</strong>finen el dolor<br />
central como quemante, constante, punzante o lacerante, en paroxismos<br />
<strong>de</strong> intensidad variable y muy poco localizados. Otro ejemplo <strong>de</strong><br />
la plasticidad funcional que se observa tras lesiones cerebrales es el<br />
hecho <strong>de</strong> que el dolor central se pue<strong>de</strong> exacerbar por sensaciones no<br />
relacionadas, cono estímulos visuales, auditivos y olfativos.<br />
El dolor central pue<strong>de</strong> durar años, puesto que no se pue<strong>de</strong> tratar<br />
con los analgésicos actuales. Para tratar el dolor central se han utilizado<br />
fármacos como los anti<strong>de</strong>presivos y los antiepilépticos, con éxito