MDCK-MRP2 - Dkfz
MDCK-MRP2 - Dkfz
MDCK-MRP2 - Dkfz
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
274<br />
Forschungsschwerpunkt E<br />
Innovative Krebsdiagnostik und -therapie<br />
Tumormobilität kranial gelegener Lungentumoren im Vergleich<br />
zu kaudal gelegenen Lungentumoren sowohl bei forcierter,<br />
wie auch ruhiger Atmung nachgewiesen werden.<br />
Durch eine frühzeitige und präzise Erfassung der Lungenmechanik<br />
hoffen wir in weiteren Untersuchungen eine<br />
weitere Präzisierung bisheriger Therapie- und Nachsorgeschemata<br />
und damit die Möglichkeit einer optimaler auf<br />
das Krankheitsstadium adaptierten Therapie erreichen zu<br />
können. Durch eine Integration dieser neuen Methoden<br />
in die Planung hochpräziser Therapietechniken scheint eine<br />
weitere Optimierung der Zielvolumendefinition mit besserer<br />
Schonung des umliegenden gesunden Gewebes möglich.<br />
[55, 98]<br />
Publikationen zum Themenkomplex Thorax, die während<br />
der Tätigkeit der Mitarbeiter an den Universitätskliniken<br />
Heidelberg und Mainz entstanden und 2002/2003 publiziert<br />
wurden: [2, 15, 17, 30, 43-46, 49, 54, 56, 58-66,<br />
81, 82, 85, 112, 114].<br />
3 Tumoren des lymphatischen Systems<br />
S. Delorme, K. Wasser<br />
Beim multiplen Myelom (MM), einer Erkrankung aus dem<br />
Formenkreis der niedrig malignen Non-Hodgkin-Lymphome,<br />
handelt es sich um eine klonale Vermehrung von Plasmazellen,<br />
die sich v.a. im blutbildenen Knochenmark manifestiert.<br />
Ein Tumorbefall kann sowohl fokal vorliegen, in Form<br />
umschriebener, den Knochen zerstörender Tumorknoten,<br />
als auch diffus. Das multiple Myelom verursacht neben<br />
umschriebenen Knochendestruktionen eine humoral vermittelte<br />
Osteoporose, eine Verdrängung des blutbildenden<br />
Knochenmarks mit den Folgen einer Anämie, Leukound<br />
Thrombopenie sowie eine fortschreitende Nierenschädigung<br />
durch glomerulär filtrierte Paraproteine.<br />
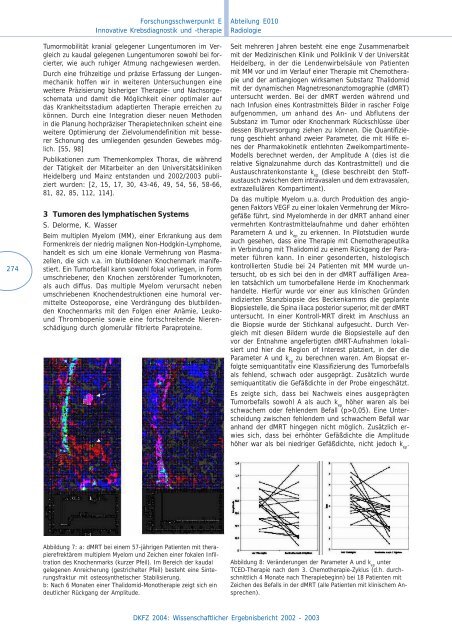
Abbildung 7: a: dMRT bei einem 57-jährigen Patienten mit therapierefrektärem<br />
multiplem Myelom und Zeichen einer fokalen Infiltration<br />
des Knochenmarks (kurzer Pfeil). Im Bereich der kaudal<br />
gelegenen Anreicherung (gestrichelter Pfeil) besteht eine Sinterungsfraktur<br />
mit osteosynthetischer Stabilisierung.<br />
b: Nach 6 Monaten einer Thalidomid-Monotherapie zeigt sich ein<br />
deutlicher Rückgang der Amplitude.<br />
Abteilung E010<br />
Radiologie<br />
Abbildung 8: Veränderungen der Parameter A und k ep unter<br />
TCED-Therapie nach dem 3. Chemotherapie-Zyklus (d.h. durchschnittlich<br />
4 Monate nach Therapiebeginn) bei 18 Patienten mit<br />
Zeichen des Befalls in der dMRT (alle Patienten mit klinischem Ansprechen).<br />
DKFZ 2004: Wissenschaftlicher Ergebnisbericht 2002 - 2003<br />
Seit mehreren Jahren besteht eine enge Zusammenarbeit<br />
mit der Medizinischen Klinik und Poliklinik V der Universität<br />
Heidelberg, in der die Lendenwirbelsäule von Patienten<br />
mit MM vor und im Verlauf einer Therapie mit Chemotherapie<br />
und der antiangiogen wirksamen Substanz Thalidomid<br />
mit der dynamischen Magnetresonanztomographie (dMRT)<br />
untersucht werden. Bei der dMRT werden während und<br />
nach Infusion eines Kontrastmittels Bilder in rascher Folge<br />
aufgenommen, um anhand des An- und Abflutens der<br />
Substanz im Tumor oder Knochenmark Rückschlüsse über<br />
dessen Blutversorgung ziehen zu können. Die Quantifizierung<br />
geschieht anhand zweier Parameter, die mit Hilfe eines<br />
der Pharmakokinetik entlehnten Zweikompartimente-<br />
Modells berechnet werden, der Amplitude A (dies ist die<br />
relative Signalzunahme durch das Kontrastmittel) und die<br />
Austauschratenkonstante k (diese beschreibt den Stoff-<br />
ep<br />
austausch zwischen dem intravasalen und dem extravasalen,<br />
extrazellulären Kompartiment).<br />
Da das multiple Myelom u.a. durch Produktion des angiogenen<br />
Faktors VEGF zu einer lokalen Vermehrung der Mikrogefäße<br />
führt, sind Myelomherde in der dMRT anhand einer<br />
vermehrten Kontrastmittelaufnahme und daher erhöhten<br />
Parametern A und k zu erkennen. In Pilotstudien wurde<br />
ep<br />
auch gesehen, dass eine Therapie mit Chemotherapeutika<br />
in Verbindung mit Thalidomid zu einem Rückgang der Parameter<br />
führen kann. In einer gesonderten, histologisch<br />
kontrollierten Studie bei 24 Patienten mit MM wurde untersucht,<br />
ob es sich bei den in der dMRT auffälligen Arealen<br />
tatsächlich um tumorbefallene Herde im Knochenmark<br />
handelte. Hierfür wurde vor einer aus klinischen Gründen<br />
indizierten Stanzbiopsie des Beckenkamms die geplante<br />
Biopsiestelle, die Spina iliaca posterior superior, mit der dMRT<br />
untersucht. In einer Kontroll-MRT direkt im Anschluss an<br />
die Biopsie wurde der Stichkanal aufgesucht. Durch Vergleich<br />
mit diesen Bildern wurde die Biopsiestelle auf den<br />
vor der Entnahme angefertigten dMRT-Aufnahmen lokalisiert<br />
und hier die Region of Interest platziert, in der die<br />
Parameter A und k zu berechnen waren. Am Biopsat er-<br />
ep<br />
folgte semiquantitativ eine Klassifizierung des Tumorbefalls<br />
als fehlend, schwach oder ausgeprägt. Zusätzlich wurde<br />
semiquantitativ die Gefäßdichte in der Probe eingeschätzt.<br />
Es zeigte sich, dass bei Nachweis eines ausgeprägten<br />
Tumorbefalls sowohl A als auch k höher waren als bei<br />
ep<br />
schwachem oder fehlendem Befall (p>0,05). Eine Unterscheidung<br />
zwischen fehlendem und schwachem Befall war<br />
anhand der dMRT hingegen nicht möglich. Zusätzlich erwies<br />
sich, dass bei erhöhter Gefäßdichte die Amplitude<br />
höher war als bei niedriger Gefäßdichte, nicht jedoch k . ep