- Page 1 and 2:
MANUALES DE REFERENCIA FARMACOLÓGI
- Page 3 and 4:
INFORMACIÓN INTRODUCTORIA Multivlt
- Page 5 and 6:
DRÍA DESCRIPCIÓN DE SECCIONES Y C
- Page 7 and 8:
INFORMACIÓN INTRODUCTORIA DEFINICI
- Page 9 and 10:
D INFORMACIÓN INTRODUCTORIA SÍMBO
- Page 11 and 12:
INFORMACIÓN INTRODUCTORIA SÍMBOLO
- Page 13 and 14:
INFORMACIÓN INTRODUCTORIA ESCRITUR
- Page 15 and 16:
PROYECTO DE DIFERENCIACIÓN DE NOMB
- Page 17 and 18:
REFERENCIAS SELECTAS Dorr RT, Von H
- Page 19 and 20:
LISTA ALFABÉTICA DE FÁRMACOS
- Page 21 and 22:
ABACAVIR Abacavir (Continúa) Vida
- Page 23 and 24:
ABACAVIR Y LAMIVUDINA Abacavir y la
- Page 25 and 26:
ABACAVIR, LAMIVUDINA Y ZIDOVUDINA A
- Page 27 and 28:
ABACAVIR, LAMIVUDINA Y ZIDOVUDINA A
- Page 29 and 30:
ACARBOSA Acarbosa (Continúa) Preca
- Page 31 and 32:
ACETAMINOFÉN Aceite mineral (Conti
- Page 33 and 34:
ACETAMINOFÉN Acetaminofén (Contin
- Page 35 and 36:
ACETAMINOFÉN Y CODEÍNA Acetaminof
- Page 37 and 38:
ACETATO DE POTASIO Acetato de calci
- Page 39 and 40:
ACETATO DE SODIO Acetato de potasio
- Page 41 and 42:
ACETAZOLAMIDA AcetaZOLAMIDA (Contin
- Page 43 and 44:
ACETILCISTEÍNA Acetilcisteína (Co
- Page 45 and 46:
ACETILCOLINA Acetilcisteína (Conti
- Page 47 and 48:
ACICLOVIR Aciclovir (Continúa) Loc
- Page 49 and 50:
ÁCIDO ACETILSALICÍLICO Aciclovir
- Page 51 and 52:
ÁCIDO ACETILSALICÍLICO Acido acet
- Page 53 and 54:
ÁCIDO AMINOCAPROICO Acido acetilsa
- Page 55 and 56:
ÁCIDO ASCÓRBICO Ácido ascórbico
- Page 57 and 58:
ÁCIDO FÓLICO Acido azelaico (Cont
- Page 59 and 60:
ACIDO FOLÍNICO (LEUCOVORÍN) Acido
- Page 61 and 62:
ÁCIDO SALICÍLICO Ácido láctico
- Page 63 and 64:
ÁCIDO TRANEXÁMICO Ácido tranexá
- Page 65 and 66:
ÁCIDO VALPROICO Y DERIVADOS Ácido
- Page 67 and 68:
ÁCIDO VALPROICO Y DERIVADOS Acido
- Page 69 and 70:
ÁCIDO ETACRÍNICO Ácido valproico
- Page 71 and 72:
APAPALENO Acido etacrínico (Contin
- Page 73 and 74:
ADENOSINA Adenosina (Continúa) Far
- Page 75 and 76:
ADRENALINA Adrenalina (Continúa) d
- Page 77 and 78:
AGALSIDASA BETA Adrenalina (Contin
- Page 79 and 80:
ALBENDAZOL Albendazol (Continúa) R
- Page 81 and 82:
1 ALBUTEROL Albuterol (Continua) Do
- Page 83 and 84:
ALBÚMINA Albúmina (Continúa) Con
- Page 85 and 86:
ALCLOMETASONA • Albúmina sérica
- Page 87 and 88:
ALCOHOL ETÍLICO Alcohol etílico (
- Page 89 and 90:
ALDESLEUCINA Alcohol etílico (Cont
- Page 91 and 92:
1 2 ALDESLEUCINA Aldesleucina (Cont
- Page 93 and 94:
ALFENTANIL Alfentanil (Continúa) P
- Page 95 and 96:
ALOPURINOL Alglucerasa (Continúa)
- Page 97 and 98:
ALPRAZOLAM Alopurínol (Continúa)
- Page 99 and 100:
ALPRAZOLAM Alprazolam (Continúa) M
- Page 101 and 102:
ALPROSTADIL Alprostadil (Continúa)
- Page 103 and 104:
ALTEPLASA Alquitrán de hulla (Cont
- Page 105 and 106:
ALTEPLASA Alteplasa (Continua) prof
- Page 107 and 108:
ALTEPLASA Alteplasa (Continúa) uti
- Page 109 and 110:
AMANTADINA Alteplasa (Continúa) Po
- Page 111 and 112:
AMIFOSTINA Amifostina (Continua) pe
- Page 113 and 114:
AMLODIPINA Amlodipina (Continúa) N
- Page 115 and 116:
AMOXICILINA • Amortiguador tris v
- Page 117 and 118:
AMOXICILINA Y ÁCIDO CLAVULÁNICO A
- Page 119 and 120:
AMPICILINA Amoxicilina y ácido cla
- Page 121 and 122:
AMPICILINA Y SULBACTAM Ampicilina (
- Page 123 and 124:
AMPRENAVIR Ampicilina y sulbactam (
- Page 125 and 126:
AMPRENAVIR Amprenavir (Continua) an
- Page 127 and 128:
ANFOTERICINA B (COMPLEJO LIPÍDICO)
- Page 129 and 130:
ANFOTERICINA B (CONVENCIONAL) Anfot
- Page 131 and 132:
ANFOTERICINA B (LIPOSÓMICA) Anfote
- Page 133 and 134:
ANTIÁCIDOS Anfotericina B (liposó
- Page 135 and 136:
ANTIPIRINA Y BENZOCAÍNA Antiácido
- Page 137 and 138:
APR0T1NINA Aprepitant (Continúa) q
- Page 139 and 140:
APROTININA Aprotinina (Continúa) D
- Page 141 and 142:
ASPAR AG1N ASA Arginina (Continúa)
- Page 143 and 144:
ATAPULGITA Asparaginasa (Continúa)
- Page 145 and 146:
ATAZANAVIR Atazanavir (Continúa) s
- Page 147 and 148:
ATAZANAVIR Atazanavir (Continúa) v
- Page 149 and 150:
ATENOLOL Atenolol (Continúa) Inter
- Page 151 and 152:
ATOMOXETINA Atomoxetina (Continua)
- Page 153 and 154:
ATORVASTATINA Atomoxetina (Continú
- Page 155 and 156:
1 ATORVASTATINA Atorvastatina (Cont
- Page 157 and 158:
ATOVACUONA Atovacuona (Continúa) G
- Page 159 and 160:
ATRACURIO Atracurio (Continúa) Rea
- Page 161 and 162:
ATROPINA Atropina (Continúa) sínd
- Page 163 and 164:
AURANOFÍN Atropina (Continúa) Sol
- Page 165 and 166:
AZELASTINA Azatioprina (Continúa)
- Page 167 and 168:
AZITROMICINA • Azidotimidina véa
- Page 169 and 170:
AZITROMICINA Azitromicina (Continua
- Page 171 and 172:
AZUFRE Y ÁCIDO SALICÍLICO Aztreon
- Page 173 and 174:
BACITRACINA Bacitracína Categoría
- Page 175 and 176:
BACLOFÉN Baclofén (Continúa) Con
- Page 177 and 178:
BECLOMETASONA Beclometasona Informa
- Page 179 and 180:
BECLOMETASONA Beclometasona (Contin
- Page 181 and 182:
BENCILPENICILOILPOLILISINA • Benc
- Page 183 and 184:
BENZOATO DE SODIO Benzatropina (Con
- Page 185 and 186:
BENZOCAÍNA Benzocaína (Continua)
- Page 187 and 188:
BERACTANT Benzocaína (Continúa) O
- Page 189 and 190:
BETAMETASONA Betametasona Informaci
- Page 191 and 192:
BETANECOL Betametasona (Continúa)
- Page 193 and 194:
BICARBONATO DE POTASIO Y CITRATO DE
- Page 195 and 196:
BICARBONATO DE SODIO Bicarbonato de
- Page 197 and 198:
BIOTINA Bicarbonato de sodio (Conti
- Page 199 and 200:
BISMUTO Bismuto (Continúa) Uso Sub
- Page 201 and 202:
BLEOMICINA Bleomicina (Continúa) e
- Page 203 and 204:
BOSENTÁN Bosentán (Continúa) pre
- Page 205 and 206:
BOSENTÁN Bosentán (Continúa) val
- Page 207 and 208:
BROMOCRIPTINA Brimonidina (Continú
- Page 209 and 210:
BROMOCRIPTINA Bromocriptina (Contin
- Page 211 and 212:
BRONFENIRAMINA Y PSEUDOEFEDRINA Bro
- Page 213 and 214:
BUDESONIDA Bronfeniramina y pseudoe
- Page 215 and 216:
BUDESONIDA Budesonida (Continúa) (
- Page 217 and 218:
BUDESONIDA Budesonida (Continúa) A
- Page 219 and 220:
BUMETANIDA Bumetanida (Continúa) s
- Page 221 and 222:
BUPRENORFINA Bupivacaína (Continú
- Page 223 and 224:
BUPRENORFINA Buprenorfina (Continú
- Page 225 and 226:
BUPRENORFINA Y NALOXONA Buprenorfin
- Page 227 and 228:
BUSPIRONA BusPIRona (Continua) vera
- Page 229 and 230:
BUSULFÁN Busulfán (Continúa) en
- Page 231 and 232:
CAFEÍNA • Butilbromuro de escopo
- Page 233 and 234:
CALAMINA Cafeína (Continúa) Otras
- Page 235 and 236:
CALCIO Calcio (Continúa) necesario
- Page 237 and 238:
CALCITRIOL Calcitonina (Continúa)
- Page 239 and 240:
CALCITRIOL Caicitriol (Continúa) I
- Page 241 and 242:
CALFACTANT Caicitriol (Continúa) C
- Page 243 and 244:
CAPTO PRIL Capsaicina (Continúa) A
- Page 245 and 246:
CARBAMACEPINA Captopril (Continúa)
- Page 247 and 248:
CARBAMACEPINA Carbamacepina (Contin
- Page 249 and 250:
CARBAMACEPINA Carbamacepina (Contin
- Page 251 and 252:
CARBINOXAMINA Carbinoxamina (Contin
- Page 253 and 254:
CARBINOXAMINA Y PSEUDOEFEDRINA Carb
- Page 255 and 256:
CARBÓN ACTIVADO Carbón activado (
- Page 257 and 258:
CARBONATO DE CALCIO Carbonato de ca
- Page 259 and 260:
CARBOPLATINO Carboplatino (Continú
- Page 261 and 262:
CARMUST1NA Carmustina (Continúa) f
- Page 263 and 264:
CARN1TINA Carnitina (Continua) indi
- Page 265 and 266:
CARVEDILOL Carvedilol (Continúa) d
- Page 267 and 268:
CARVEDILOL Carvedilol (Continúa) n
- Page 269 and 270:
CASPOFUNGINA Caspofungina Informaci
- Page 271 and 272:
CEFACLOR Cefaclor (Continúa) Contr
- Page 273 and 274:
CEFALEXINA Cefadroxil (Continua) Ad
- Page 275 and 276:
CEFAZOLINA Cefazolina (Continúa) L
- Page 277 and 278:
CEFDINIR Cefdinir (Continúa) Renal
- Page 279 and 280:
CEFEPIMA Cefepima (Continúa) Niño
- Page 281 and 282:
CEFOTAXIMA Cefixima (Continua) Dosi
- Page 283 and 284:
CEFOTETÁN Cefotaxima (Continúa) I
- Page 285 and 286:
CEFOXITINA Cefoxitina (Continúa) R
- Page 287 and 288:
CEFPROZIL Cefpodoxima (Continúa) V
- Page 289 and 290:
CEFRAD1NA Cefradina (Continúa) Con
- Page 291 and 292:
CEFTIZOXIMA Ceftazidima (Continúa)
- Page 293 and 294:
CEFTRIAXONA Ceftriaxona (Continúa)
- Page 295 and 296:
CEFUROXIMA Cefuroxima (Continúa) K
- Page 297 and 298:
CETIRIZINA Cetirizina (Continúa) H
- Page 299 and 300:
CIANOCOB ALAMINA Cianocobalamina (C
- Page 301 and 302:
CICLOBENZAPRINA Ciclobenzaprina Sin
- Page 303 and 304:
CICLOFOSF AMIDA Ciclofosfamida (Con
- Page 305 and 306:
CICLOPENTOLATO Y FENILEFRINA Ciclop
- Page 307 and 308:
CICLOSPORINA CicloSERINA (Continúa
- Page 309 and 310:
CICLOSPORINA CicloSPORINA (Continú
- Page 311 and 312:
CIDOFOVIR CicloSPORINA (Continúa)
- Page 313 and 314:
CIMETIDINA Cidofovir (Continúa) Ma
- Page 315 and 316:
CIPROFLOXACINA Cimetidina (Continú
- Page 317 and 318:
CIPROFLOXACINA Ciprofloxacina (Cont
- Page 319 and 320:
C1PR0FL0XAC1NA Ciprofloxacina (Cont
- Page 321 and 322:
CIPROHEPTADINA Ciprofloxacina y dex
- Page 323 and 324:
CISAPRIDA Cisaprida (Continúa) rep
- Page 325 and 326:
1 CISATRACURIO Cisatracurio (Contin
- Page 327 and 328:
CISPLATINO Cisplatino (Continúa) n
- Page 329 and 330:
CISTEÍNA Cisteamina (Continúa) Ó
- Page 331 and 332:
CITALOPRAM Citalopram (Continúa) S
- Page 333 and 334:
CITALOPRAM Citalopram (Continúa) M
- Page 335 and 336:
CITARABINA Citarabina Información
- Page 337 and 338:
CITRATO DE MAGNESIO Citrato de calc
- Page 339 and 340:
CLADRIBINA Citrato y ácido cítric
- Page 341 and 342:
CLARITROMICINA Cladribina (Continú
- Page 343 and 344:
Clindamicina CLINDAMICINA Interacci
- Page 345 and 346:
CLINDAMICINA > 2 000 g : 15 mg/kg/d
- Page 347 and 348:
CLOBETASOL Duac: almacenar en refri
- Page 349 and 350:
379 CLOBETASOL Espuma, loción: apl
- Page 351 and 352:
CLONACEPAM Parámetros para vigilan
- Page 353 and 354:
CLONIDINA se estudia; la utilidad d
- Page 355 and 356:
CLONIDINA intervalo usual de dosifi
- Page 357 and 358:
CLORAMBUCIL dosis 3.75 mg cada sema
- Page 359 and 360:
Información adicional Efecto mielo
- Page 361 and 362:
Clorfeniramina Alertas especiales C
- Page 363 and 364:
CL0RHEXID1NA Clorhexidina Sinónimo
- Page 365 and 366:
CLORHIDRATO DE /.-ASPARTATO DE MAGN
- Page 367 and 368:
Farmacocinética Metabolismo: las e
- Page 369 and 370:
CLOROPROMACINA Farmacodinamia Inici
- Page 371 and 372:
CLOROQUINA Sistema nervioso central
- Page 373 and 374:
CLOROTIACIDA Oculares: visión borr
- Page 375 and 376:
CLORURO DE CALCIO Presentaciones La
- Page 377 and 378:
CLORURO DE POTASIO Complemento diet
- Page 379 and 380:
CLORURO DE SODIO ondas eventuales o
- Page 381 and 382:
Clorzoxazona CLORZOXAZONA Solución
- Page 383 and 384:
COCAÍNA Distribución: luego de su
- Page 385 and 386:
CODEÍNA levorfanol, oxicodona, oxi
- Page 387 and 388:
COLESTIRAMINA Diálisis: no dializa
- Page 389 and 390:
COLISTIMETATO Tonstad S, Knudtzon J
- Page 391 and 392:
COMPLEJO COAGULANTE ANTIINHIBIDOR f
- Page 393 and 394:
CORTICOTROPINA Interacción con ali
- Page 395 and 396:
COSINTROPINA Interacción con alime
- Page 397 and 398:
CROMOLÍN Sinónimos Ácido cromogl
- Page 399 and 400:
CROTAMITÓN Solución oftálmica, c
- Page 401 and 402:
Reacciones adversas Cardiovasculare
- Page 403 and 404:
Vida media: Niños: 13 días Adulto
- Page 405 and 406:
Inyectable, polvo para reconstituir
- Page 407 and 408:
DANTROLENO estudio aleatorizado, do
- Page 409 and 410:
DAPSONA casos publicados han utiliz
- Page 411 and 412:
DARBEP0YET1NA ALFA Información par
- Page 413 and 414:
DARBEPOYETINA ALFA anticuerpos. La
- Page 415 and 416:
1 DAUNORRUBICINA Prueba Frecuencia
- Page 417 and 418:
DEFERASIROX Implicaciones para la a
- Page 419 and 420:
DEFEROXAMINA Administración Oral:
- Page 421 and 422:
DEFEROXAMINA dosis subsecuentes de
- Page 423 and 424:
DESIMIPRAMINA Distribución: se dis
- Page 425 and 426:
DESIMIPRAMINA niños que reciben >
- Page 427 and 428:
DESLORATADINA claritromicina u otro
- Page 429 and 430:
Terminal: 75.5 min (intervalo: 0.4
- Page 431 and 432:
DEXAMETASONA aparato respiratorio,
- Page 433 and 434:
DEXMEDETOMIDINA Dexametasona, neomi
- Page 435 and 436:
DEXRAZOXANO Biodisponibilidad: IM:
- Page 437 and 438:
DEXTRÁN Swain SM, et al. Cardiopro
- Page 439 and 440:
DEXTRANFETAMINA Advertencias Existe
- Page 441 and 442:
DEXTRANFETAMINA Y ANFETAMINA sínto
- Page 443 and 444:
DEXTRANFETAMINA Y ANFETAMINA Divers
- Page 445 and 446:
DEXTRANFETAMINA Y ANFETAMINA de ale
- Page 447 and 448:
DEXTROMETORFÁN Para información a
- Page 449 and 450:
DEXTROSA Factor de riesgo para el e
- Page 451 and 452:
DIACEPAM Categoría terapéutica Ag
- Page 453 and 454:
DIACEPAM Nota: redondear la dosis a
- Page 455 and 456:
DIBUCAÍNA el diazóxido puede aume
- Page 457 and 458:
DICLOFENACO tránsito gastrointesti
- Page 459 and 460:
Estabilidad Solución oftálmica: a
- Page 461 and 462:
DICLOXACILiNA Broncoscopia: usar 2
- Page 463 and 464:
DIDANOSINA mortales. Evitar el uso
- Page 465 and 466:
DIDANOSINA < 60 kg: 125 mg cada 12
- Page 467 and 468:
DIFENHIDRAMINA La segundad y eficac
- Page 469 and 470:
DIFENOXILATO Y ATROPINA Crema, como
- Page 471 and 472:
DIGOXINA Dosificación pediátrica
- Page 473 and 474:
DIGOXINA Biodisponibilidad: (depend
- Page 475 and 476:
DIHIDROERGOTAMINA Puede incrementar
- Page 477 and 478:
DILTIACEM Presentaciones La informa
- Page 479 and 480:
R11 DILTIACEM Tabletas de liberaci
- Page 481 and 482:
DIMERCAPROL exantema, enrojecimient
- Page 483 and 484:
DIPIRIDAMOL vasodilatación; tambi
- Page 485 and 486:
DISOPIRAMIDA Disopiramida Informaci
- Page 487 and 488:
• d-manitol véase Manitoi en la
- Page 489 and 490:
DOCUSATO Y SENNA • Docusato calci
- Page 491 and 492:
Unión a proteínas: 69 a 77% (meta
- Page 493 and 494:
DORNASA ALFA Dosis alta: > 15 ug/kg
- Page 495 and 496:
DOXACURIO Disminución promedio de
- Page 497 and 498:
DOXAPRAM Disfunción renal: 3.7 h D
- Page 499 and 500:
DOXEPINA Depresión del SNC inducid
- Page 501 and 502:
DOXEPINA Cardiovasculares: hipotens
- Page 503 and 504:
DOXICICLINA Lactancia Se excreta en
- Page 505 and 506:
DOXOrrubicina DOXORRUBICINA Paráme
- Page 507 and 508:
DOXORRUBICINA Terminal: 17 a 30 h p
- Page 509 and 510:
DROPERIDOL Biodisponibilidad: 10 a
- Page 511 and 512:
DROTRECOGINA ALFA (ACTIVADA) Inform
- Page 513 and 514:
EDETATO DISÓDICO Smith KJ, Neal J,
- Page 515 and 516:
EDETATO DISÓDICO DE CALCIO Informa
- Page 517 and 518:
EDROFONIO Referencias American Acad
- Page 519 and 520:
EFAVIRENZ Factor de riesgo para el
- Page 521 and 522:
EFAVIRENZ después sufren glucuroni
- Page 523 and 524:
EFEDRINA anestesia con halotano y c
- Page 525 and 526:
EMTRICITABINA Respiratorias: tos, r
- Page 527 and 528:
ENALAPRIL Sinónimos Enalaprilato;
- Page 529 and 530:
ENALAPRIL 2.5 a 40 mg/día dividido
- Page 531 and 532:
• Enalaprilato véase Enalapn! en
- Page 533 and 534:
ENOXAPARINA frascos reconstituidos
- Page 535 and 536:
ENOXAPARINA Sistema nervioso centra
- Page 537 and 538:
EP1NASTINA La sobredosificación ac
- Page 539 and 540:
EPOPROSTENOL Los síntomas de sobre
- Page 541 and 542:
EPOPROSTENOL domicilio. Puede utili
- Page 543 and 544:
EPOYETINA ALFA vascular, isquemia,
- Page 545 and 546:
Ajuste de dosis de epoyetina alfa E
- Page 547 and 548:
ERGOCALCIFEROL Solución inyectable
- Page 549 and 550:
ERGOTAMINA Presentaciones La inform
- Page 551 and 552:
ERGOTAMINA Y CAFEÍNA Advertencias
- Page 553 and 554:
ERITROMICINA Óticas: ototoxicidad
- Page 555 and 556:
ERITROMICINA Y SULFISOXAZOL Present
- Page 557 and 558:
ERTAPENEM Administración Oral: adm
- Page 559 and 560:
Referencias Curran M, Simpson D, Pe
- Page 561 and 562:
ESMOLOL EsmoloS Información relaci
- Page 563 and 564:
ESOMEPRAZOL Vincent RN, Click LA, W
- Page 565 and 566:
ESPIRONOLACTONA mezcla con 50 mL de
- Page 567 and 568:
Estanozolol ESTANOZOLOL cereza para
- Page 569 and 570:
ESTAVUDINA Estavudina Información
- Page 571 and 572:
Cápsulas: 15 mg, 20, 30 mg, 40 mg
- Page 573 and 574:
ESTRADIOL si el complemento se admi
- Page 575 and 576:
ESTREPTOCINASA Aloran [parche dos v
- Page 577 and 578:
ESTREPTOMICINA Estreptomicina Infor
- Page 579 and 580:
ESTRÓGENOS (CONJUGADOS, EQUINOS) i
- Page 581 and 582:
ETAMBUTOL tabletas de Ovral^ de inm
- Page 583 and 584:
ETANERCEPT Etanercept Categoría te
- Page 585 and 586:
ETIDRONATO DISÓDICO Uso Tratamient
- Page 587 and 588:
ETOMIDATO Implicaciones para ia ate
- Page 589 and 590:
ETOPÓSIDO Precauciones Usar con ca
- Page 591 and 592:
ETOSUXIMIDA Contraindicaciones Hipe
- Page 593:
EZETIMIBA de ios quelantes de ácid
- Page 596 and 597:
FAB INMUNOLÓGICO ANTICROTAÜCO (PO
- Page 598 and 599:
FAB INMUNOLÓGICO CONTRA DIGOXINA F
- Page 600 and 601:
FACTOR VIIA (RECOMBINANTE) FAB inmu
- Page 602 and 603:
FACTOR IX Factor IX (Continúa) Con
- Page 604 and 605:
FACTOR IX, COMPLEJO (HUMANO) Factor
- Page 606 and 607:
FACTOR ANTIHEMOFÍLICO/FACTOR DE VO
- Page 608 and 609:
FACTOR ANTIHEMOFÍLICO (HUMANO) Fac
- Page 610 and 611:
FACTOR ANTIHEMOFÍLICO (HUMANO) Fac
- Page 612 and 613:
1 FACTOR ANTIHEMOFÍLICO (RECOMBINA
- Page 614 and 615:
FACTOR ANTIHEMOFÍLICO (RECOMBINANT
- Page 616 and 617:
FAMCICLOVIR Famciclovir (Continúa)
- Page 618 and 619:
FAM0TID1NA Famotidina (Continúa) (
- Page 620 and 621:
FELBAMATO Felbamato Información re
- Page 622 and 623:
FENAZ0PIRID1NA Felbamato (Continúa
- Page 624 and 625:
FENILACETATO DE SODIO Y BENZOATO DE
- Page 626 and 627:
FENILEFRINA Fenilbutirato de sodio
- Page 628 and 629:
FENILEFRINA Fenilefrina (Continúa)
- Page 630 and 631:
FENITOÍNA Fenitoína (Continúa) m
- Page 632 and 633:
FENITOÍNA Fenitoína (Continúa) A
- Page 634 and 635:
FENOBARBITAL Fenobarbitai (Continú
- Page 636 and 637:
FENTANIL Fenoxibenzamina (Continúa
- Page 638 and 639:
FENTANIL Fentanil (Continúa) unida
- Page 640 and 641:
FENTANIL Fentanil (Continúa) Durac
- Page 642 and 643:
FENTANIL Fentanil (Continúa) Admin
- Page 644 and 645:
FENTANIL Fentanil (Continúa) conoc
- Page 646 and 647:
FENTOLAMINA Fentolamina (Continúa)
- Page 648 and 649:
FILGRASTIM Fexofenadina (Continúa)
- Page 650 and 651:
FISOSTIGMINA Filgrastim (Continua)
- Page 652 and 653:
FITONADIONA Fitonadiona (Continúa)
- Page 654 and 655:
FLECAINIDA Flecainida (Continua) De
- Page 656 and 657:
FLUCITOSINA administración concurr
- Page 658 and 659:
FLUCONAZOL Fluconazol (Continúa) j
- Page 660 and 661:
FLUDARABINA Fluconazol (Continúa)
- Page 662 and 663:
FLUDROCORTISONA Fludarabina (Contin
- Page 664 and 665:
FLUMAZENIL Flumazenil (Continúa) i
- Page 666 and 667:
FLUNISOLIDA Flunisolida (Continúa)
- Page 668 and 669:
FLUOCINOLONA Fiunisolída (Continú
- Page 670 and 671:
FLUOCINONIDA Fluocinolona (Continú
- Page 672 and 673:
FLUOROURACILO Fluorouracilo Informa
- Page 674 and 675:
FLUOXETINA Fluorouracilo (Continúa
- Page 676 and 677:
FLUOXETINA Fluoxetina (Continúa) v
- Page 678 and 679:
FLUOXETINA Fluoxetina (Continua) la
- Page 680 and 681:
FLURACEPAM Fluoximesterona (Contin
- Page 682 and 683:
FLURBIPROFÉN Fluracepam (Continúa
- Page 684 and 685:
FLUTICASONA Fluticasona (Continúa)
- Page 686 and 687:
FLUTICASONA Fluticasona (Continúa)
- Page 688 and 689:
FLUTICASONA Fluticasona (Continúa)
- Page 690 and 691:
1 FLUTICASONA Y SALMETEROL Fluticas
- Page 692 and 693:
FLUVOXAMINA Fluvoxamina (Continúa)
- Page 694 and 695:
FLUVOXAMINA Fluvoxamina (Continúa)
- Page 696 and 697:
FLÚOR Fluvoxamina (Continúa) Levi
- Page 698 and 699:
FOMEPIZOL Flúor (Continúa) Gel, t
- Page 700 and 701:
FORMOTEROL Fomepizol (Continúa) Do
- Page 702 and 703:
FOSAMPRENAVIR Formoterol (Continúa
- Page 704 and 705:
FOSAMPRENAVIR Fosamprenavir (Contin
- Page 706 and 707:
FOSCARNET Foscarnet (Continúa) Rea
- Page 708 and 709:
FOSFATO DE POTASIO Fosfato (Contin
- Page 710 and 711:
FOSFATO DE POTASIO Fosfato de potas
- Page 712 and 713:
FOSFATO DE POTASIO Y FOSFATO DE SOD
- Page 714 and 715:
FOSFATO DE SODIO Fosfato de sodio (
- Page 716 and 717:
FOSFATO TRIBÁSICO DE CALCIO Fosfat
- Page 718 and 719:
FOSFENITOÍNA Fosfenitoína (Contin
- Page 720 and 721:
FUROSEMIDA Fosfenitoína (Continúa
- Page 722 and 723:
FUROSEMIDA Furosemida (Continúa) l
- Page 724 and 725:
1 2 GABAPENTINA Gabapentina (Contin
- Page 726 and 727:
GANCICLOVIR Gancicíovir (Continua)
- Page 728 and 729:
GENTAMICINA Gancicíovir Referencia
- Page 730 and 731:
GENTAMICINA Gentamicina (Continúa)
- Page 732 and 733:
GLIBURIDA GliBURIDA (Continúa) Lac
- Page 734 and 735:
GLICERINA GMBURIDA (Continúa) Refe
- Page 736 and 737:
GLIPIZIDA GlipiZIDA (Continúa) Rea
- Page 738 and 739:
GLOBULINA ANTITIMOCITO (DE CONEJO)
- Page 740 and 741:
GLUBIONATO DE CALCIO Globulina anti
- Page 742 and 743:
GLUCONATO DE CALCIO Glucagon (sinte
- Page 744 and 745:
GLUCONATO DE MAGNESIO Gluconato de
- Page 746 and 747:
GLUCOPIRROLATO Gluconato de potasio
- Page 748 and 749:
GONADORRELINA Gonadorrelina (Contin
- Page 750 and 751:
GRANISETRÓN Gonadotropina corióni
- Page 752 and 753:
GRISEOFULVINA Granisetrón (Contin
- Page 754 and 755:
GUAIFENESINA Guaifenesina (Continú
- Page 756 and 757:
GUAIFENESINA Y DEXTROMETORFÁN Guai
- Page 758 and 759:
GUAIFENESINA Y DEXTROMETORFÁN Guai
- Page 760 and 761:
HALOPERIDOL Halobetasol (Continua)
- Page 762 and 763:
HEMORROIDALES Haloperidol (Continú
- Page 764 and 765:
HEPARINA Heparina (Continúa) ("sí
- Page 766 and 767:
HEPARINA Heparina (Continúa) Admin
- Page 768 and 769:
HEXACLOROFENOL Hetaalmidón (Contin
- Page 770 and 771:
HIDRALAZINA Hialuronidasa (Continú
- Page 772 and 773:
HIDRATO DE CLORAL HidrALAZINA (Cont
- Page 774 and 775:
HIDROCLOROTIACIDA Hidrato de cloral
- Page 776 and 777:
HIDROCLOROTIACIDA Y ESPIRONOLACTONA
- Page 778 and 779:
HIDROCORTISONA Hidrocodona y acetam
- Page 780 and 781:
HIDROCORTISONA Hidrocortisona (Cont
- Page 782 and 783:
HIDROMORFONA Hidrocortisona (Contin
- Page 784 and 785:
HIDROMORFONA Hidromorfona (Continú
- Page 786 and 787:
HIDROXICLOROQIJINA Hidroxicloroquin
- Page 788 and 789:
HIDR0XIC0BALAWI1NA Hidroxicobalamin
- Page 790 and 791:
HIDROXIUREA Hidroxicobalamina (Cont
- Page 792 and 793:
HIDROXIZINA Hidroxiurea (Continúa)
- Page 794 and 795:
HIDRÓXIDO DE MAGNESIO HidrOXIZINA
- Page 796 and 797:
HIERRO (COMPLEMENTOS ORALES Y ENTÉ
- Page 798 and 799:
HIERRO (COMPLEMENTOS PARENTERALES)
- Page 800 and 801: HIERRO (COMPLEMENTOS PARENTERALES)
- Page 802 and 803: HIOSCIAMINA Hiosciamina (Continúa)
- Page 804 and 805: HOMATROPINA Hiosciamina, atropina,
- Page 806 and 807: HORMONA DE CRECIMIENTO HUMANA Hormo
- Page 808 and 809: HORMONA DE CRECIMIENTO HUMANA Hormo
- Page 810 and 811: IBUPROFÉN Ibuprofén (Continúa) E
- Page 812 and 813: IBUPROFÉN Ibuprofén (Continúa) H
- Page 814 and 815: IBUPROFÉN Ibuprofén (Continúa) P
- Page 816 and 817: IDARRUBICINA I b u p roté n (Con t
- Page 818 and 819: IFOSFAMIDA Idarrubicina (Continua)
- Page 820 and 821: IMIGLUCERASA Imiglucerasa (Continú
- Page 822 and 823: IMIPENEM Y CILASTATINA Imipenem y c
- Page 824 and 825: I MI PR AMINA Imipramina (Continúa
- Page 826 and 827: INAMRINONA Inamrínona Sinónimos A
- Page 828 and 829: INDINAVIR Inamrinona (Continúa) Gu
- Page 830 and 831: INDINAVIR Indinavir (Continúa) Far
- Page 832 and 833: INDOMETACINA Indometacina (Continú
- Page 834 and 835: INFLIXIMAB Infliximab Sinónimos Fa
- Page 836 and 837: INMUNOGLOBULINA ANTIRH-(D) Inflixim
- Page 838 and 839: INMUNOGLOBULINA ANTIRH 0(D) Inmunog
- Page 840 and 841: INMUNOGLOBULINA ANTIRRÁBICA (HUMAN
- Page 842 and 843: INMUNOGLOBULINA BOTULÍNICA HUMANA
- Page 844 and 845: INMUNOGLOBULINA CONTRA CITOMEGALOVI
- Page 846 and 847: INMUNOGLOBULINA CONTRA VIRUS VARICE
- Page 848 and 849: INMUNOGLOBULINA (INTRAMUSCULAR) Inm
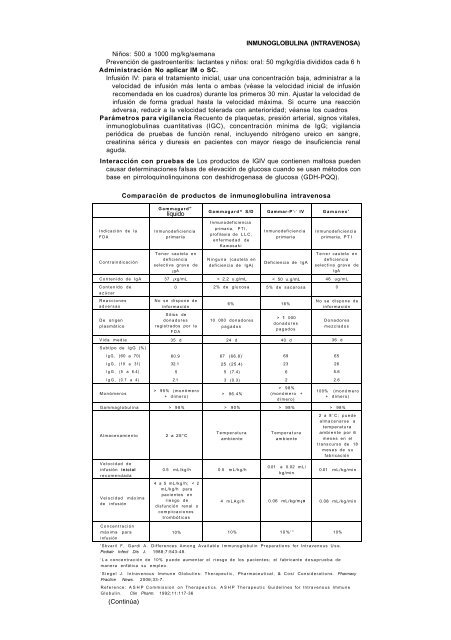
- Page 852 and 853: INMUNOGLOBULINA (INTRAVENOSA) Inmun
- Page 854 and 855: INSULINA ASPÁRTICA PROTAMINA E INS
- Page 856 and 857: INSULINA GLARGINA Insulina detemir
- Page 858 and 859: INSULINA INHALADA Insulina glulisin
- Page 860 and 861: INSULINA LISPRO Insulina inhalada (
- Page 862 and 863: INSULINA NPH Insulina lispro protam
- Page 864 and 865: INSULINA REGULAR Insulina NPH e ins
- Page 866 and 867: INSULINA REGULAR Insulina regular (
- Page 868 and 869: INSULINA REGULAR Insulina regular (
- Page 870 and 871: INTERFERÓN ALFA-2A Interíerón al
- Page 872 and 873: INTERFERÓN ALFA-2B Interferón alf
- Page 874 and 875: IPECACUANA interferon alfa-2b (Cont
- Page 876 and 877: IPRATROPIO I p ratrop i o (Continú
- Page 878 and 879: IRINOTECÁN Irinotecán (Continúa)
- Page 880 and 881: ISONIAZIDA Isoniazida (Continúa) L
- Page 882 and 883: ISOPROTERENOL Isoproterenol Informa
- Page 884 and 885: IS0TRET1N0ÍNA Isotretinoína (Cont
- Page 886 and 887: ISRADIPINA isradipina (Continúa) G
- Page 888 and 889: ITRACONAZOL Isradipina (Continúa)
- Page 890 and 891: KETAMINA Itraconazol (Continúa) In
- Page 892 and 893: KETOCONAZOL Ketamina (Continúa) Im
- Page 894 and 895: KETOROLACO Ketoconazol (Continúa)
- Page 896 and 897: KETOROLACO Ketoroíaco (Continúa)
- Page 898 and 899: KETOTIFENO Ketotifeno Sinónimos Fu
- Page 900 and 901:
LABETALOL Labetalol (Continua) Dura
- Page 902 and 903:
LACTATO DE CALCIO Lactato de calcio
- Page 904 and 905:
LACTULOSA Lactobacillus acidophilus
- Page 906 and 907:
LAMIVUDINA Lamivudina (Continúa) P
- Page 908 and 909:
LAMIVUDINA Y ZIDOVUDINA Lamivudina
- Page 910 and 911:
LAMOTRIGINA Lamotrigina (Continua)
- Page 912 and 913:
LAMOTRIGINA Lamotrigina (Continúa)
- Page 914 and 915:
LAMOTRIGINA Lamotrigina (Continúa)
- Page 916 and 917:
LANSOPRAZOL Lansoprazol (Continúa)
- Page 918 and 919:
LARONIDASA Lansoprazol (Continúa)
- Page 920 and 921:
LEUPROLIDA • /-carnitina véase C
- Page 922 and 923:
LEVALBUTEROL Leuprolida (Continúa)
- Page 924 and 925:
LEVETIRACETAM Levetiracetam (Contin
- Page 926 and 927:
LEVETIRACETAM Levetiracetam (Contin
- Page 928 and 929:
LEVODOPA Levodopa Información rela
- Page 930 and 931:
LEVOFLOXACINA Levofloxacina (Contin
- Page 932 and 933:
LEVOTIROXINA Levofloxacina (Contin
- Page 934 and 935:
LEVOTIROXINA Levotiroxina (Continú
- Page 936 and 937:
LIDOCAÍNA Lidocaína (Continúa) e
- Page 938 and 939:
LIDOCAÍNA Y EPINEFRINA Lidocaína
- Page 940 and 941:
LIDOCAÍNA Y PRILOCAÍNA Lidocaína
- Page 942 and 943:
LINDANO Lidocaína y prilocaína (C
- Page 944 and 945:
LINEZOLID Lindano (Continua) Es pos
- Page 946 and 947:
LINEZOLID Linezolid (Continúa) Vid
- Page 948 and 949:
LIOTIRONINA Liotironina (Continúa)
- Page 950 and 951:
LISINOPRIL Lisinopril (Continúa) m
- Page 952 and 953:
LITIO Litio (Continúa) Sinónimos
- Page 954 and 955:
LOMUSTINA Litio (Continúa) niveles
- Page 956 and 957:
LOPERAMIDA Lomustina (Continúa) Re
- Page 958 and 959:
LOPINAVIR Y RITONAVIR Lopinavir y r
- Page 960 and 961:
LOPINAVIR Y RITONAVIR Lopinavir y r
- Page 962 and 963:
LORACEPAM Loracarbef (Continúa) tr
- Page 964 and 965:
LORACEPAM Loracepam (Continúa) •
- Page 966 and 967:
LORATADINA Y PSEUDOEFEDRINA Loratad
- Page 968 and 969:
LOVASTATINA Lovastatina Sinónimos
- Page 970 and 971:
LUBRICANTE OFTÁLMICO Lovastatina (
- Page 972 and 973:
MAFENIDA Lípidos en emulsión (Con
- Page 974 and 975:
MAGNESIO Magnesio (Continúa) Trata
- Page 976 and 977:
MANITOL • Maleato de timolol véa
- Page 978 and 979:
MECLIZINA Mebendazol (Continúa) Pa
- Page 980 and 981:
MEDRISONA Mecloretamina (Continúa)
- Page 982 and 983:
MEDROXIPROGESTERONA Medroxiprogeste
- Page 984 and 985:
MEFLOOUINA Mefloquina (Continúa) I
- Page 986 and 987:
MEGESTROL Mefobarbital (Continúa)
- Page 988 and 989:
MELFALÁN Megestrol (Continúa) Par
- Page 990 and 991:
MEPERIDINA Melfalán (Continúa) Pl
- Page 992 and 993:
MEPERIDINA Meperidina (Continúa) N
- Page 994 and 995:
MERCAPTOPURINA Mepivacaína (Contin
- Page 996 and 997:
MEROPENEM Mercaptopurina (Continúa
- Page 998 and 999:
MESALAMINA Meropenem (Continúa) In
- Page 1000 and 1001:
MES NA Mesalamina (Continua) Suspen
- Page 1002 and 1003:
METADONA Metadona (Continúa) espec
- Page 1004 and 1005:
METADONA Metadona (Continúa) Niño
- Page 1006 and 1007:
Metaproterenol (Continúa) Duració
- Page 1008 and 1009:
METFORMINA Metformina Sinónimos Cl
- Page 1010 and 1011:
METILDOPA Metformina (Continúa) In
- Page 1012 and 1013:
METILFENIDATO Metildopa (Continua)
- Page 1014 and 1015:
METILFENIDATO Metilfenidato (Contin
- Page 1016 and 1017:
METILFENIDATO Metilfenidato (Contin
- Page 1018 and 1019:
METILPREDNISOLONA Metilfenidato (Co
- Page 1020 and 1021:
METILPREDNISOLONA MetilPREDNISolona
- Page 1022 and 1023:
METIRAPONA Metimazol (Continúa) Ad
- Page 1024 and 1025:
METOCLOPR AMIDA Metocarbamol (Conti
- Page 1026 and 1027:
METOHEXITAL Metoclopramida (Contin
- Page 1028 and 1029:
METOLAZONA Metohexital (Continúa)
- Page 1030 and 1031:
METOPROLOL Metoprolol Información
- Page 1032 and 1033:
METOPROLOL Metoprolol (Continúa) e
- Page 1034 and 1035:
METOTREXATE Metosuximida (Continúa
- Page 1036 and 1037:
METOTREXATE Metotrexate (Continúa)
- Page 1038 and 1039:
METRONIDAZOL Metotrexate (Continúa
- Page 1040 and 1041:
MEXILETINA Metronidazol (Continúa)
- Page 1042 and 1043:
MICAFUNGÍN Micafungín (Continúa)
- Page 1044 and 1045:
MICOFENOLATO Micofenolato (Continú
- Page 1046 and 1047:
MICONAZOL Micofenolato (Continúa)
- Page 1048 and 1049:
MIDAZOLAM Miconazol (Continúa) Mon
- Page 1050 and 1051:
MIDAZOLAM Midazolam (Continúa) Not
- Page 1052 and 1053:
MILRINONA Midazolam (Continua) para
- Page 1054 and 1055:
MILRINONA Milrinona (Continúa) Inf
- Page 1056 and 1057:
MISOPROSTOL Minoxidil (Continúa) D
- Page 1058 and 1059:
MITOMICINA Mitomicina (Continúa) C
- Page 1060 and 1061:
MITOXANTRONA Mitoxantrona (Continua
- Page 1062 and 1063:
MIVACURIO Mivacurio (Continúa) Res
- Page 1064 and 1065:
MOMETASONA Mometasona (Continúa) g
- Page 1066 and 1067:
MOMETASONA Mometasona (Continúa) r
- Page 1068 and 1069:
MORFINA Montelukast (Continúa) Tie
- Page 1070 and 1071:
MORFINA Morfina (Continúa) intrarr
- Page 1072 and 1073:
MORFINA Morfina (Continúa) Farmaco
- Page 1074 and 1075:
MORFINA Morfina (Continúa) liberac
- Page 1076 and 1077:
MUPIROCÍN « MTC véase Mitomicina
- Page 1078 and 1079:
NABILONA Muromonab-CD3 (Continúa)
- Page 1080 and 1081:
NADOLOL • A/-acetilcisteína véa
- Page 1082 and 1083:
NAFCILINA Nafazolina (Continua) Adm
- Page 1084 and 1085:
NALBUF1NA Nafcilina (Continúa) Inf
- Page 1086 and 1087:
NALOXONA Nalbufina (Continúa) Kend
- Page 1088 and 1089:
NANDROLONA Naloxona (Continúa) Inf
- Page 1090 and 1091:
NAPROXÉN Naproxén (Continúa) Sin
- Page 1092 and 1093:
NAPROXÉN Naproxén (Continúa) Dos
- Page 1094 and 1095:
NELARABINA Nedocromil (Continúa) H
- Page 1096 and 1097:
NELFINAVIR Nelarabina (Continúa) D
- Page 1098 and 1099:
NELFINAVIR Nelfinavir (Continúa) M
- Page 1100 and 1101:
NEOMICINA, POLIMIXINA B E HIDROCORT
- Page 1102 and 1103:
NEOMICINA, POLIXIMINA B Y PREDNISOL
- Page 1104 and 1105:
NEOSTIGMINA Neostigmina (Continúa)
- Page 1106 and 1107:
NEVIRAPINA Nevirapina (Continúa) v
- Page 1108 and 1109:
NIACINA Nevirapina (Continúa) Muel
- Page 1110 and 1111:
NIACINA Niacina (Continua) 500 mg/d
- Page 1112 and 1113:
NIFEDÍPINA NIFEdipina (Continúa)
- Page 1114 and 1115:
NITAZOXANIDA Nistatina (Continúa)
- Page 1116 and 1117:
NITIS1NONA Nitisinona (Continúa) P
- Page 1118 and 1119:
NITRITO DE SODIO, TIOSULFATO DE SOD
- Page 1120 and 1121:
NITROFURANTOÍNA Nitrito de sodio,
- Page 1122 and 1123:
NITROGLICERINA Nitrofurantoína (Co
- Page 1124 and 1125:
NITROPRUSIATO Nitroglicerina (Conti
- Page 1126 and 1127:
NIZATIDINA Nizatidina (Continúa) P
- Page 1128 and 1129:
NORETINDRONA Noradrenalina (Continu
- Page 1130 and 1131:
NORTRIPTILINA Nortriptilina (Contin
- Page 1132 and 1133:
NORTRIPTILINA Nortriptilina (Contin
- Page 1134 and 1135:
OCTREÓTIDO Octreótido (Continúa)
- Page 1136 and 1137:
OFLOXACINA Octreótido (Continúa)
- Page 1138 and 1139:
OFLOXACINA Ofloxacina (Continua) Do
- Page 1140 and 1141:
OLIGOELEMENTOS Oligoelementos (Cont
- Page 1142 and 1143:
OLSALAZINA Oligoelementos (Continú
- Page 1144 and 1145:
OMALIZUMAB Omalizumab (Continúa) r
- Page 1146 and 1147:
OMEPRAZOL Omeprazol (Continúa) Adv
- Page 1148 and 1149:
ONDANSETRÓN Omeprazol (Continúa)
- Page 1150 and 1151:
OPRELVEKÍN Ondansetrón (Continúa
- Page 1152 and 1153:
ORO Oprelvekín (Continúa) Efecto
- Page 1154 and 1155:
OSELTAMIVIR Oseltamivir (Continúa)
- Page 1156 and 1157:
OXACILINA Oxacilina Sinónimos Meti
- Page 1158 and 1159:
OXALIPLATINO Oxaliplatino (Continú
- Page 1160 and 1161:
OXAPROZINA Oxaprozina (Continúa) P
- Page 1162 and 1163:
OXCARBACEPINA Oxaprozina (Continúa
- Page 1164 and 1165:
OXCARBACEPINA Oxcarbacepina (Contin
- Page 1166 and 1167:
OXIBUTININA Oxibutinina (Continúa)
- Page 1168 and 1169:
OXICODONA Oxicodona (Continúa) Gen
- Page 1170 and 1171:
OXICODONA Y ACETAMINOFÉN Oxicodona
- Page 1172 and 1173:
ÓXIDO DE MAGNESIO Oxicodona y áci
- Page 1174 and 1175:
OXIMETAZOLINA Oximetazolina Informa
- Page 1176 and 1177:
PACLITAXEL Paclitaxel (Continúa) D
- Page 1178 and 1179:
PALONOSETRÓN Palivizumab (Continua
- Page 1180 and 1181:
PAMIDRONATO Pamidronato (Continúa)
- Page 1182 and 1183:
PAN CREATINA Pamoato de pirantel (C
- Page 1184 and 1185:
PANCREOLIPASA Pancreatina (Continú
- Page 1186 and 1187:
PANCURONIO Pancreolipasa (Continúa
- Page 1188 and 1189:
PANTOPRAZOL Pancuronio (Continúa)
- Page 1190 and 1191:
PAPAVERINA Pantoprazol (Continúa)
- Page 1192 and 1193:
PAREGÓRICO Paregórico Informació
- Page 1194 and 1195:
PARICALCITOL Paricalcitol (Continua
- Page 1196 and 1197:
PAROMOMICINA Parlcalcitol (Continú
- Page 1198 and 1199:
PAROXETINA Paroxetina (Continúa) U
- Page 1200 and 1201:
PAROXETINA Paroxetina (Continúa) m
- Page 1202 and 1203:
PAROXETINA Paroxetina (Continúa) a
- Page 1204 and 1205:
PEGASPARGASA Pegaspargasa (Continú
- Page 1206 and 1207:
PENCICLOVIR Penciclovir Sinónimos
- Page 1208 and 1209:
PENICILAMINA Penicilamina (Continú
- Page 1210 and 1211:
PENICILINA G BENZATÍNICA Penicilin
- Page 1212 and 1213:
PENICILINA G (PARENTERAL/ACUOSA) Pe
- Page 1214 and 1215:
PENICILINA G PROCAÍNICA Penicilina
- Page 1216 and 1217:
PENTAMIDINA Pentamidina (Continua)
- Page 1218 and 1219:
PENTOBARBITAL Pentazocina (Continú
- Page 1220 and 1221:
PENTOXIFILINA Pentobarbital (Contin
- Page 1222 and 1223:
PERMETRINA Pentoxifilina (Continúa
- Page 1224 and 1225:
PERÓXIDO DE CARBAMIDA Peróxido de
- Page 1226 and 1227:
PIL0CARP1NA Peróxido de hidrógeno
- Page 1228 and 1229:
PIMECROLIMUS Pimecrolimus (Continú
- Page 1230 and 1231:
PIPERACILINA Y TAZOBACTAM Piperacil
- Page 1232 and 1233:
PIPERACILINA Y TAZOBACTAM Piperacil
- Page 1234 and 1235:
PIRBUTEROL Pirazinamida (Continúa)
- Page 1236 and 1237:
PIRIDOSTIGMINA Piridostigmina (Cont
- Page 1238 and 1239:
PIRIMETAMINA Piridoxina (Continúa)
- Page 1240 and 1241:
PIROXICAM Pirimetamina (Continúa)
- Page 1242 and 1243:
POLIETILENGLICOL EN SOLUCIÓN ELECT
- Page 1244 and 1245:
POLIMIXINA B Polietilenglicol en so
- Page 1246 and 1247:
PORACTANTE ALFA Polimixina B (Conti
- Page 1248 and 1249:
POSACONAZOL Posaconazol (Continúa)
- Page 1250 and 1251:
PRAVAST ATINA Pravastatina Sinónim
- Page 1252 and 1253:
PRAZIQUANTEL Pravastatina (Continú
- Page 1254 and 1255:
PREDNISOLONA Prazosín (Continúa)
- Page 1256 and 1257:
PREDNISOLONA PrednisoLONA (Continú
- Page 1258 and 1259:
PREDNISOLONA Y GENTAMICINA Predniso
- Page 1260 and 1261:
PREDNISONA PredniSONA Oral-. (Conti
- Page 1262 and 1263:
PRIMIDONA Primaquina (Continúa) Do
- Page 1264 and 1265:
PROBENECID Probenecid (Continua) Ga
- Page 1266 and 1267:
PROCAIN AMIDA Procainamida (Contin
- Page 1268 and 1269:
PROCARBAZINA Procainamida (Continua
- Page 1270 and 1271:
PROCAÍNA Procaína (Continúa) Lac
- Page 1272 and 1273:
PROCLORPERAZINA Proclorperazina (Co
- Page 1274 and 1275:
PROMETAZINA Prometazina (Continúa)
- Page 1276 and 1277:
PROMETAZINA, FENILEFRINA Y CODEÍNA
- Page 1278 and 1279:
PROMETAZINA Y FENILEFRINA Prometazi
- Page 1280 and 1281:
PROPARACAÍNA Propantelina (Contin
- Page 1282 and 1283:
PROPOFOL Propiltiouracilo (Continú
- Page 1284 and 1285:
PROPOFOL Propofol (Continua) Su sup
- Page 1286 and 1287:
PROPOXIFENO Propofol (Continúa) ge
- Page 1288 and 1289:
PROPRANOLOL Propoxifeno y acetamino
- Page 1290 and 1291:
PROPRANOLOL Propranolol (Continúa)
- Page 1292 and 1293:
PROTAMINA • Prostaglandina E-, v
- Page 1294 and 1295:
PSEUDOEFEDRINA Protirelina (Continu
- Page 1296 and 1297:
PSEUDOEFEDRINA E IBUPROFÉN Pseudoe
- Page 1298 and 1299:
PSYLLIUM Psyllium (Continúa) Lacta
- Page 1300 and 1301:
QUINIDINA Quinidina (Continua) nece
- Page 1302 and 1303:
QUININA Quinina (Continúa) Puede e
- Page 1304 and 1305:
QUINUPRISTINA Y DALFOPRISTINA Quinu
- Page 1306 and 1307:
RANITIDINA Rabeprazol (Continúa) E
- Page 1308 and 1309:
RANITIDINA Ranitidina (Continua) Vi
- Page 1310 and 1311:
RASBURICASA Rasburicasa (Continúa)
- Page 1312 and 1313:
REMIFENTANIL Remifentanil (Continú
- Page 1314 and 1315:
RIBAVIRINA • rtHuEPO-a véase Epo
- Page 1316 and 1317:
RIBAVIRINA Ribavirina (Continúa) d
- Page 1318 and 1319:
RIBOFLAVINA Ribavirina (Continúa)
- Page 1320 and 1321:
RIFAMPICINA Rifabutina (Continúa)
- Page 1322 and 1323:
RIFAMPICINA Rifampicina (Continúa)
- Page 1324 and 1325:
RISPERIDONA Rimantadina (Continua)
- Page 1326 and 1327:
RISPERIDONA Risperidona (Continúa)
- Page 1328 and 1329:
RISPERIDONA Risperidona (Continúa)
- Page 1330 and 1331:
RISPERIDONA Risperidona (Continua)
- Page 1332 and 1333:
RITONAVIR Risperidona (Continúa) S
- Page 1334 and 1335:
RITONAVIR Ritonavir (Continúa) Cá
- Page 1336 and 1337:
RITUXIMAB Rituximab (Continúa) Adv
- Page 1338 and 1339:
ROCURONIO Rituximab (Continúa) Omi
- Page 1340 and 1341:
ROPIVACAÍNA Rocuronio (Continúa)
- Page 1342 and 1343:
ROSIGLITAZONA Ropivacaína (Contin
- Page 1344 and 1345:
ROSIGLITAZONA Rosiglitazona (Contin
- Page 1346 and 1347:
SALMETEROL Sacarosidasa (Continúa)
- Page 1348 and 1349:
SAQUINAVIR Salmeterol (Continúa) R
- Page 1350 and 1351:
SAQUINAVIR Saquinavir (Continúa) D
- Page 1352 and 1353:
SARGRAMOSTIM Sargramostim (Continú
- Page 1354 and 1355:
SECOBARBITAL Secobarbital (Continú
- Page 1356 and 1357:
SECRETINA Secretina (Continúa) Est
- Page 1358 and 1359:
SERTRALINA Senna (Continúa) Tablet
- Page 1360 and 1361:
SERTRALINA Sertralina (Continúa) N
- Page 1362 and 1363:
SERTRALINA Sertralina (Continúa) a
- Page 1364 and 1365:
1 SIMETICONA Sevelamer (Continúa)
- Page 1366 and 1367:
SINVASTATINA Sinvastatina (Continua
- Page 1368 and 1369:
SIROLIMUS Sinvastatina (Continúa)
- Page 1370 and 1371:
SORBITOL Sirolimus (Continúa) Admi
- Page 1372 and 1373:
SOTALOL Sotalol (Continua) referenc
- Page 1374 and 1375:
SOTALOL Sotaíol (Continua) recomen
- Page 1376 and 1377:
SOTALOL Sotalol (Continúa) Betapac
- Page 1378 and 1379:
SUCCINILCOLINA Succímero (Continua
- Page 1380 and 1381:
SUCRALFATO Sucralfato (Continúa) o
- Page 1382 and 1383:
SUERO CONTRA LATRODECTUS MACTANS Su
- Page 1384 and 1385:
SU FENTANIL Sufentanil (Continúa)
- Page 1386 and 1387:
SULFADIAZINA Sulfacetamida (Contin
- Page 1388 and 1389:
SULFADIAZINA ARGÉNTICA Sulfadiazin
- Page 1390 and 1391:
SULFAMETOXAZOL Y TRIMETOPRIM Sulfad
- Page 1392 and 1393:
SULFASALAZINA Sulfametoxazol y trim
- Page 1394 and 1395:
SULFATO DE MAGNESIO Sulfasalazina (
- Page 1396 and 1397:
SULFATO DE MAGNESIO Sulfato de magn
- Page 1398 and 1399:
SULFONATO SÓDICO DE POLIESTIRENO S
- Page 1400 and 1401:
SUL1NDAC Sulfuro de selenio (Contin
- Page 1402 and 1403:
SUMATRIPTÁN Sumatriptán (Continua
- Page 1404 and 1405:
TACROLIMUS Sumatriptán (Continúa)
- Page 1406 and 1407:
TACROLIMUS Tacrolimus (Continúa) M
- Page 1408 and 1409:
TAZAROTENO Tazaroteno (Continúa) l
- Page 1410 and 1411:
TEMOZOLOMIDA Temozolomída (Contin
- Page 1412 and 1413:
TENOFOVIR Tenipósido (Continúa) s
- Page 1414 and 1415:
TENOFOVIR Tenofovir (Continúa) El
- Page 1416 and 1417:
TEOFILINA Tenofovir (Continúa) tem
- Page 1418 and 1419:
2 3 TEOFILINA Teofilina (Continúa)
- Page 1420 and 1421:
TEOFILINA Teofilina (Continúa) Dos
- Page 1422 and 1423:
TESTOSTERONA Terbutalina (Continúa
- Page 1424 and 1425:
TESTOSTERONA Testosterona (Continú
- Page 1426 and 1427:
TETRACAÍNA Tetracaína (Continua)
- Page 1428 and 1429:
TETRACICLINA Tetraciclina (Continú
- Page 1430 and 1431:
TIAGABINA Tiabendazol (Continúa) P
- Page 1432 and 1433:
TIAMINA Tiagabina (Continúa) Infor
- Page 1434 and 1435:
TICARCILINA Ticarcilina Sinónimos
- Page 1436 and 1437:
TICARCILINA Y CLAVULANATO POTÁSICO
- Page 1438 and 1439:
TIMOLOL Timolol (Continua) hiperten
- Page 1440 and 1441:
TINTURA DE OPIO Tintura de opio (Co
- Page 1442 and 1443:
TIOPENTAL Tioguanina (Continúa) Do
- Page 1444 and 1445:
TIORIDAZINA Tiopental (Continúa) I
- Page 1446 and 1447:
TIOSULFATO DE SODIO Tiosulfato de s
- Page 1448 and 1449:
TIOTEPA Tiotepa (Continúa) TEPA: 1
- Page 1450 and 1451:
TIOTROPIO Tiotropio Sinónimos Brom
- Page 1452 and 1453:
TOBRAMICINA Tobramicina (Continúa)
- Page 1454 and 1455:
TOLMETINA Tobramicina (Continúa) P
- Page 1456 and 1457:
TOLNAFTATO Tolmetina (Continúa) Ro
- Page 1458 and 1459:
TOPIR AMATO Topiramato (Continúa)
- Page 1460 and 1461:
TOPOTECÁN Topiramato (Continúa) m
- Page 1462 and 1463:
TORSEMIDA Topotecán (Continúa) Re
- Page 1464 and 1465:
TOXINA BOTULÍNICA TIPO A Toxina bo
- Page 1466 and 1467:
TOXINA BOTULÍNICA TIPO B Toxina bo
- Page 1468 and 1469:
3 5 TOXOIDES DE DIFTERIA Y TÉTANOS
- Page 1470 and 1471:
3 s TRAMADOL Toxoide tetánico (con
- Page 1472 and 1473:
TRAZODONA Tramadol (Continúa) Meta
- Page 1474 and 1475:
TRAZODONA Trazodona (Continúa) Car
- Page 1476 and 1477:
TRIAMCINOLONA Tretinoína (Continú
- Page 1478 and 1479:
TRIAMCINOLONA Triamcinolona (Contin
- Page 1480 and 1481:
TRIAZOLAM Triamtireno (Continúa) D
- Page 1482 and 1483:
TRIAZOLAM Triazolam (Continúa) lop
- Page 1484 and 1485:
TRIGLICÉRIDOS DE CADENA MEDIA Trif
- Page 1486 and 1487:
TRIMETOBENZAMIDA Trihexifenidil (Co
- Page 1488 and 1489:
TRIMETOPRIM Trimetobenzamida (Conti
- Page 1490 and 1491:
TRIPR0L1DINA Y PSEUDOEFEDRINA Trime
- Page 1492 and 1493:
TROMBINA Trisalicilato de colina y
- Page 1494 and 1495:
TROPICAMIDA Trometamina (Continúa)
- Page 1496 and 1497:
URSODIOL Ursodiol (Continúa) Mecan
- Page 1498 and 1499:
VACUNA ANTINEUMOCÓCICA CONJUGADA (
- Page 1500 and 1501:
VACUNA ANTIRRÁBICA Vacuna antineum
- Page 1502 and 1503:
VACUNA CONJUGADA CONTRA DIFTERIA, T
- Page 1504 and 1505:
VACUNA CONJUGADA CONTRA HAEMOPHILUS
- Page 1506 and 1507:
VACUNA CONTRA DIFTERIA, TÉTANOS, T
- Page 1508 and 1509:
VACUNA CONTRA DIFTERIA, TÉTANOS Y
- Page 1510 and 1511:
VACUNA CONTRA HEPATITIS A Vacuna co
- Page 1512 and 1513:
VACUNA CONTRA HEPATITIS B Vacuna co
- Page 1514 and 1515:
VACUNA CONTRA INFLUENZA (VIRUS INAC
- Page 1516 and 1517:
VACUNA CONTRA INFLUENZA (VIRUS INAC
- Page 1518 and 1519:
VACUNA CONTRA PAROTIDITIS (VIRUS VI
- Page 1520 and 1521:
VACUNA CONTRA POLIOMIELITIS (VIRUS
- Page 1522 and 1523:
VACUNA CONTRA ROTAVIRUS (VIRUS VIVO
- Page 1524 and 1525:
VACUNA CONTRA SARAMPIÓN, PAROTIDIT
- Page 1526 and 1527:
VACUNA CONTRA SARAMPIÓN, PAROTIDIT
- Page 1528 and 1529:
VACUNA CONTRA SARAMPIÓN, PAROTIDIT
- Page 1530 and 1531:
VACUNA CONTRA VARICELA Vacuna contr
- Page 1532 and 1533:
VACUNA CONTRA VIRUS DE ENCEFALITIS
- Page 1534 and 1535:
VACUNA CONTRA VIRUS DEL PAPILOMA (R
- Page 1536 and 1537:
VACUNA DE POLISACÁRIDO MENINGOCÓC
- Page 1538 and 1539:
VALACICLOVIR Vacuna de polisacárid
- Page 1540 and 1541:
VALACICLOVIR Valaciclovir (Continú
- Page 1542 and 1543:
VALGANCICLOVIR Valganciclovir (Cont
- Page 1544 and 1545:
VANCOMICINA Vancomicina (Continúa)
- Page 1546 and 1547:
VASOPRESINA Vasopresina Interaccion
- Page 1548 and 1549:
VECURONIO Vecuronio (Continúa) Con
- Page 1550 and 1551:
VENLAFAXINA Venlafaxina (Continua)
- Page 1552 and 1553:
VENLAFAXINA Venlafaxina (Continúa)
- Page 1554 and 1555:
VENLAFAXINA Venlafaxina (Continúa)
- Page 1556 and 1557:
VERAPAMIL Verapamil (Continúa) Dú
- Page 1558 and 1559:
VINBLASTINA Verapamil (Continúa) T
- Page 1560 and 1561:
VINCRISTINA VinBLAStina (Continua)
- Page 1562 and 1563:
VIOLETA DE GENCIANA Violeta de genc
- Page 1564 and 1565:
VITAMINA E Vitamina A (Continúa) S
- Page 1566 and 1567:
VORICONAZOL Voriconazol Informació
- Page 1568 and 1569:
VORICONAZOL Voriconazol (Continúa)
- Page 1570 and 1571:
WARFARINA Warfarina (Continúa) gra
- Page 1572 and 1573:
WARFARINA Warfarina (Continúa) Dos
- Page 1574 and 1575:
YODIXANOL Warfarina (Continua) mole
- Page 1576 and 1577:
YODO Yodixanoi (Continúa) Niños d
- Page 1578 and 1579:
YODURO DE POTASIO Yodoquinol (Conti
- Page 1580 and 1581:
YODURO DE POTASIO Y YODO Yoduro de
- Page 1582 and 1583:
ZAFIRLUKAST Zafirlukast (Continúa)
- Page 1584 and 1585:
ZALCITABINA Zalcitabina (Continúa)
- Page 1586 and 1587:
ZIDOVUDINA Zidovudina (Continúa) r
- Page 1588 and 1589:
ZIDOVUDINA Zidovudina (Continúa) I
- Page 1590 and 1591:
ZINC Zinc (Continúa) Complemento p
- Page 1592 and 1593:
ZONISAMIDA Zonisamida (Continúa) I
- Page 1594 and 1595:
CARDIOLOGÍA DOSIFICACIÓN DE FÁRM
- Page 1596 and 1597:
CALCULO DE LA VELOCIDAD PARA INFUSI
- Page 1598 and 1599:
CARDIOLOGÍA seis" calcula la dosis
- Page 1600 and 1601:
CARDIOLOGÍA FRECUENCIA CARDIACA NO
- Page 1602 and 1603:
MEDICIÓN DE LA PRESIÓN ARTERIAL E
- Page 1604 and 1605:
CARDIOLOGÍA HIPOTENSIÓN, DEFINICI
- Page 1606 and 1607:
PRESIÓN ARTERIAL NORMAL EN NEONATO
- Page 1608 and 1609:
CARDIOLOGÍA Valores de presión ar
- Page 1610 and 1611:
Presión arterial en NIÑO, según
- Page 1612 and 1613:
Presión arterial en NINAS, según
- Page 1614 and 1615:
2 a 1 Presión arterial en NIÑAS,
- Page 1616 and 1617:
CARDIOLOGÍA CLASIFICACIÓN DE LA C
- Page 1618 and 1619:
CITOCROMO P450 Y METABOLISMO DE FÁ
- Page 1620 and 1621:
CITOCROMO P450 Y METABOLISMO DE FÁ
- Page 1622 and 1623:
CITOCROMO P450 Y METABOLISMO DE FÁ
- Page 1624 and 1625:
CITOCROMO P450 Y METABOLISMO DE FÁ
- Page 1626 and 1627:
CITOCROMO P450 Y METABOLISMO DE FÁ
- Page 1628 and 1629:
CITOCROMO P450 Y METABOLISMO DE FÁ
- Page 1630 and 1631:
CITOCROMO P450 Y METABOLISMO DE FÁ
- Page 1632 and 1633:
CITOCROMO P450 Y METABOLISMO DE FÁ
- Page 1634 and 1635:
CITOCROMO P450 Y METABOLISMO DE FÁ
- Page 1636 and 1637:
GRÁFICAS DE CRECIMIENTO FUENTE: De
- Page 1638 and 1639:
Gráficas de crecimiento de los CDC
- Page 1640 and 1641:
Gráficas de crecimiento de los CDC
- Page 1642 and 1643:
RFrFMiPWTn Y DESARROLLO Gráficas d
- Page 1644 and 1645:
CRECIMIENTO Y DESARROLLO Nacimiento
- Page 1646 and 1647:
CÁLCULO DEL PESO CORPORAL IDEAL Ad
- Page 1648 and 1649:
CRECIMIENTO Y DESARROLLO PESO Y ÁR
- Page 1650 and 1651:
TRATAMIENTO EN CASO DE EXTRAVASACI
- Page 1652 and 1653:
MANEJO DE QUEMADURAS Modificado del
- Page 1654 and 1655:
Comparación de dosis usuales para
- Page 1656 and 1657:
DOSIFICACIÓN DATOS COMPARATIVOS CO
- Page 1658 and 1659:
DOSIFICACIÓN DATOS COMPARATIVOS Co
- Page 1660 and 1661:
PRODUCTOS MULTIVITAMNICOS (ORALES Y
- Page 1662 and 1663:
AquADEKs [OTC] Producto AquADEKs [O
- Page 1664 and 1665:
Fórmulas multlvitamínlcas pediát
- Page 1666 and 1667:
Fórmulas multivitamínicas pediát
- Page 1668 and 1669:
Formulaciones prenatales (continua)
- Page 1670 and 1671:
Formulaciones prenatales (continúa
- Page 1672 and 1673:
Formulaciones prenatales (continúa
- Page 1674 and 1675:
Fórmulas multivitamínicas para ad
- Page 1676 and 1677:
Producto B, (mg) Fórmulas de compl
- Page 1678 and 1679:
Fórmulas de complejo B para adoles
- Page 1680 and 1681:
I DATOS COMPARATIVOS PREPARADOS OTC
- Page 1682 and 1683:
DOSIFICACIÓN DATOS COMPARATIVOS De
- Page 1684 and 1685:
ANTICONCEPTIVOS ORALES ENDOCRINOLOG
- Page 1686 and 1687:
Anticonceptivos orales monofásicos
- Page 1688 and 1689:
HEMATOLOGÍA Y ONCOLOGÍA COMPATIBI
- Page 1690 and 1691:
HEMATOLOGÍA Y ONCOLOGÍA Compatibl
- Page 1692 and 1693:
HEMATOLOGÍA Y ONCOLOGÍA Compatibl
- Page 1694 and 1695:
HEMATOLOGÍA Y ONCOLOGÍA Compatibl
- Page 1696 and 1697:
Incompatible: SN Anfotericina Amsac
- Page 1698 and 1699:
Incompatible: Alopurinol Cefepima D
- Page 1700 and 1701:
Compatible; G 5 inromgatible: Gemci
- Page 1702 and 1703:
Compatible mediante arimin stració
- Page 1704 and 1705:
Mecloretamína Mesna Metoclopramida
- Page 1706 and 1707:
HEMATOLOGÍA Y ONCOLOGÍA Sargramos
- Page 1708 and 1709:
HEMATOLOGÍA Y ONCOLOGÍA Cotrimoxa
- Page 1710 and 1711:
uPMAmi ^GJA Y ONCOLOGÍA Carboplati
- Page 1712 and 1713:
UEMATYM ng¡ A y ONCOLOGÍA TRATAMI
- Page 1714 and 1715:
HEMATOLOGÍA Y ONCOLOGÍA 1.2.2. El
- Page 1716 and 1717:
HEMATOLOGÍA Y ONCOLOGÍA 1.12 Prof
- Page 1718 and 1719:
de PC, cuando esté disponible, en
- Page 1720 and 1721:
HEPATOLOGÍA EVALUACIÓN DE LA FUNC
- Page 1722 and 1723:
Cuadro 2. Procedimientos dentales y
- Page 1724 and 1725:
INFECTOLOGÍA E INMUNOLOGÍA Cuadro
- Page 1726 and 1727:
Indicaciones para el inicio de tera
- Page 1728 and 1729:
INFECTOLOGIA E INMUNOLOGÍA Element
- Page 1730 and 1731:
INFECTOLOGÍA E INMUNOLOGÍA Facili
- Page 1732 and 1733:
INFECTOLOGÍA E INMUNOLOGÍA Indica
- Page 1734 and 1735:
Componentes antirretrovirales acept
- Page 1736 and 1737:
Regímenes o componentes antirretro
- Page 1738 and 1739:
INFECTOLOGÍA E INMUNOLOGÍA Resume
- Page 1740 and 1741:
Recomendaciones para realización d
- Page 1742 and 1743:
VIH PERINATAL Cuadros selectos toma
- Page 1744 and 1745:
INFECTOLOGÍA E INMUNOLOGÍA minimi
- Page 1746 and 1747:
• El cumplimiento óptimo del ré
- Page 1748 and 1749:
INFECTOLOGÍA E INMUNOLOGÍA LINEAM
- Page 1750 and 1751:
Lineamientos para dosificación y a
- Page 1752 and 1753:
INFECTOLOGÍA E INMUNOLOGÍA se ini
- Page 1754 and 1755:
Regímenes recomendados para la vac
- Page 1756 and 1757:
! 1 Esquema de inmunización recome
- Page 1758 and 1759:
Esquema de actualización recomenda
- Page 1760 and 1761:
8 9 Varicela (edad mínima: 12 mese
- Page 1762 and 1763:
INFECTOLOGÍA E INMUNOLOGÍA Lineam
- Page 1764 and 1765:
Recomendaciones para la inmunizaci
- Page 1766 and 1767:
PALUDISMO Dosis para adultos Dosis
- Page 1768 and 1769:
Tratamiento del paludismo Fármaco
- Page 1770 and 1771:
Tratamiento del paludismo (continú
- Page 1772 and 1773:
2 3 5 8 9 ,1 1 2 1 3 Para infeccion
- Page 1774 and 1775:
Vacuna General para todas las vacun
- Page 1776 and 1777:
Hepatitis B Hepatitis A Varicela VP
- Page 1778 and 1779:
INFECTOLOGÍA E INMUNOLOGÍA PRUEBA
- Page 1780 and 1781:
INFECTOLOGÍA E INMUNOLOGÍA MANEJO
- Page 1782 and 1783:
Profilaxia posterior a la exposici
- Page 1784 and 1785:
INFECTOLOGÍA E INMUNOLOGÍA Situac
- Page 1786 and 1787:
INFECTOLOGÍA E INMUNOLOGÍA Manejo
- Page 1788 and 1789:
Regímenes básico y expandido de p
- Page 1790 and 1791:
INFECTOLOGÍA E INMUNOLOGÍA que de
- Page 1792 and 1793:
Toxicidad grave (p. ej., nefrolitia
- Page 1794 and 1795:
LABORATORIO, VALORES DE REFERENCIA
- Page 1796 and 1797:
LABORATORIO, VALORES DE REFERENCIA
- Page 1798 and 1799:
Edad GB (x 10 3 /mm 3 ) Leucocitos
- Page 1800 and 1801:
LÍQUIDOS, ELECTRÓLITOS Y NUTRICI
- Page 1802 and 1803:
LÍQUIDOS, ELECTRÓLITOS Y NUTRICI
- Page 1804 and 1805:
LÍQUIDOS, ELECTRÓLITOS Y NUTRICI
- Page 1806 and 1807:
LÍQUIDOS, ELECTRÓLITOS Y NUTRICI
- Page 1808 and 1809:
Fórmula de soya 1 (Indicaciones: m
- Page 1810 and 1811:
LÍQUIDOS, ELECTRÓLITOS Y NUTRICI
- Page 1812 and 1813:
LÍQUIDOS, ELECTRÓLITOS Y NUTRICI
- Page 1814 and 1815:
FORMULAS ENTÉRALES — PEDIÁTRICA
- Page 1816 and 1817:
LÍQUIDOS, ELECTRÓLITOS Y NUTRICI
- Page 1818 and 1819:
LÍQUIDOS, ELECTRÓLITOS Y NUTRICI
- Page 1820 and 1821:
LÍQUIDOS, ELECTRÓLITOS Y NUTRICI
- Page 1822 and 1823:
LÍQUIDOS, ELECTRÓLITOS Y NUTRICI
- Page 1824 and 1825:
LÍQUIDOS, ELECTRÓLITOS Y NUTRICI
- Page 1826 and 1827:
LÍQUIDOS, ELECTRÓLITOS Y NUTRICI
- Page 1828 and 1829:
LÍQUIDOS, ELECTRÓLITOS Y NUTRICI
- Page 1830 and 1831:
LÍQUIDOS, ELECTRÓLITOS Y NUTRICI
- Page 1832 and 1833:
LÍQUIDOS, ELECTRÓLITOS Y NUTRICI
- Page 1834 and 1835:
Niños de 1 a 18 años El siguiente
- Page 1836 and 1837:
MECOQLOGI'A obstrucción aguda de v
- Page 1838 and 1839:
CALIFICACIÓN DE APGAR Calificació
- Page 1840 and 1841:
ASMA Adaptado de: National Asthma E
- Page 1842 and 1843:
NEUMOLOGÍA • En general, el uso
- Page 1844 and 1845:
NEUROLOGÍA En cada paso los pacien
- Page 1846 and 1847:
TRATAMIENTO DE EXACERBACIONES DEL A
- Page 1848 and 1849:
NEUMOLOGÍA 400 a 800 ug/día (dosi
- Page 1850 and 1851:
FRECUENCIA RESPIRATORIA NORMAL Hora
- Page 1852 and 1853:
NEUROLOGÍA PREMEDICACIÓN SEDANTE
- Page 1854 and 1855:
Fármaco Ketamina Sedantes empleado
- Page 1856 and 1857:
NEUROLOGÍA irritabilidad), trastor
- Page 1858 and 1859:
8. Dependencia de piridoxina 9. Ano
- Page 1860 and 1861:
NEUROLOGÍA ESCALAS DEL COMA Escala
- Page 1862 and 1863:
NIVELES TERAPÉUTICOS DE FÁRMACOS
- Page 1864 and 1865:
Fármaco o clase de fármaco Benzod
- Page 1866 and 1867:
Fármaco o clase de fármaco Antide
- Page 1868 and 1869:
Agente venenoso Antídoto(s) Indica
- Page 1870 and 1871:
Agente venenoso Antídoto(s) Indica
- Page 1872 and 1873:
Agente venenoso Antfdoto(s) Indicac
- Page 1874 and 1875:
Agente venenoso Antídoto(s) Indica
- Page 1876 and 1877:
TOXICOLOGÍA ANÁLISIS PARA DETECCI
- Page 1878 and 1879:
TOXICOLOGÍA INTOXICACIÓN POR SALI
- Page 1880 and 1881:
MEDICAMENTOS DE LOS QUE UNA SOLA DO
- Page 1882 and 1883:
Cuadro 3. Compuestos radiactivos qu
- Page 1884 and 1885:
TEMAS DIVERSOS LACTANCIA Y FÁRMACO
- Page 1886 and 1887:
TEMAS DIVERSOS LACTANCIA Y FÁRMACO
- Page 1888 and 1889:
COMPATIBILIDAD DE MEDICAMENTOS MEZC
- Page 1890 and 1891:
FIEBRE POR USO DE FÁRMACOS Mas com
- Page 1892 and 1893:
TEMAS DIVERSOS CAMBIO DE COLORACIÓ
- Page 1894 and 1895:
USO DE FÁRMACOS DURANTE EL EMBARAZ
- Page 1896 and 1897:
ADMINISTRACIÓN DE MEDICAMENTOS EN
- Page 1898 and 1899:
TEMAS DIVERSOS ADMINISTRACIÓN DE M
- Page 1900 and 1901:
TEMAS DIVERSOS ADMINISTRACIÓN DE M
- Page 1902 and 1903:
TEMAS DIVERSOS SÍNDROME SEROTONIN
- Page 1904 and 1905:
TEMAS DIVERSOS SÍNDROME SEROTONIN
- Page 1906 and 1907:
TEMAS DIVERSOS SÍNDROME SEROTONIN
- Page 1908 and 1909:
TEMAS DIVERSOS MEDICAMENTOS ORALES
- Page 1910 and 1911:
TEMAS DIVERSOS PREPARACIONES DE USO
- Page 1912 and 1913:
TEMAS DIVERSOS PREPARACIONES DE USO
- Page 1914 and 1915:
TEMAS DIVERSOS CONTENIDO DE CARBOHI
- Page 1916 and 1917:
TEMAS DIVERSOS CONTENIDO DE CARBOHI
- Page 1918 and 1919:
TEMAS DIVERSOS CONTENIDO DE CARBOHI
- Page 1920 and 1921:
TEMAS DIVERSOS CONTENIDO DE CARBOHI
- Page 1922 and 1923:
TEMAS DIVERSOS CONTENIDO DE CARBOHI
- Page 1924 and 1925:
TEMAS DIVERSOS CONTENIDO DE CARBOHI
- Page 1926 and 1927:
TEMAS DIVERSOS MEDICAMENTOS ORALES
- Page 1928 and 1929:
TEMAS DIVERSOS MEDICAMENTOS ORALES
- Page 1930 and 1931:
TEMAS DIVERSOS MEDICAMENTOS ORALES
- Page 1932:
TEMAS DIVERSOS MEDICAMENTOS ORALES